MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Allergische Rhinitis
Der Allergische Marsch – wie aktuell ist er heute?
Eltville (24. Mai 2013) – Viel zu oft wird die in Europa häufigste atopische Erkrankung [1], die Allergische Rhinitis, bagatellisiert. Das hat fatale Folgen – denn wenn sie „Karriere macht“, kann es zu ernsten, die Lebensqualität und das Leistungsvermögen einschränkenden Komplikationen kommen [2]. Die Rede ist vom allergischen Marsch, der sich von der Nahrungsmittelunverträglichkeit mit drohender Anaphylaxiegefahr über die atopische Dermatitis bis hin zum Asthma bronchiale erstreckt. Trotz dieses hohen Risikopotenzials werde ein Großteil der Patienten mit Allergischer Rhinitis unzureichend therapiert, so dass sie keine befriedigende Verbesserung ihrer Beschwerden erleben [3], berichtet Prof. Dr. med. Ludger Klimek, Leiter des Allergiezentrums Wiesbaden anlässlich des MEDA-Fachsymposiums während der diesjährigen „Allergologie im Kloster“-Tagung.
Eine frühzeitige Behandlung des allergischen Marsches ist sinnvoll um die Versorgung der Patienten zu verbessern und den sozioökonomischen Druck zu reduzieren. Zielgerichtete Behandlungsstrategien sowie Schulungsprogramme für Patienten zur Vermeidung der akuten Situation sind notwendig, die mit hoher Wirksamkeit und schnellem Wirkeintritt eine nahezu vollständige Symptombefreiung erreichen. Die Zulassung des neuen rezeptpflichtigen und erstattungsfähigen Arzneimittels Dymista® im März dieses Jahres betrachten Klimek und seine Co-Referenten Prof. Dr. med. Knut Brockow, München und Dr. med. Jörg Fischer, Tübingen, als einen wesentlichen Schritt in diese Richtung. Dymista ist ein neuartiges Nasenspray, bestehend aus dem Antihistaminikum Azelastin und dem Kortikoid Fluticason. In dem umfangreichen Studienprogramm mit annähernd 5000 Patienten zeigte sich die Überlegenheit des neuen Präparates gegenüber den Einzelsubstanzen, insbesondere was die schnelle und umfassende Reduktion der nasalen und okularen Symptome bei Patienten mit mittelschwerer bis schwere saisonaler oder perennialer Allergischer Rhinitis anbelangt.
In den internationalen Leitlinien gilt die Anwendung von Antihistaminika und topischen Glukokortikosteroiden bei intermittierender und persistierender Allergischer Rhinitis (AR) als therapeutischer Standard. Die Realität für deutsche Allergie-Patienten sieht allerdings anders aus: Nur rund ein Drittel der Patienten erhält ein Medikament vom Arzt rezeptiert, ein weiteres Drittel betreibt Selbstmedikation und die übrigen werden nicht therapiert [4]. Angesichts der Häufigkeit der Erkrankung und ihrer ernsten gesundheitlichen Auswirkungen sei das nicht länger hinnehmbar, so Brockow während seines Vortrags. Zumal auch der volkswirtschaftliche Schaden zu berücksichtigen ist, bedenkt man, dass durch die unbehandelte AR höhere Einbußen an Arbeitsproduktivität entstehen, als bei Diabetes, Asthma oder Depressionen [5].
Mit ein Grund für die unbefriedigende Therapiesituation ist in den erheblichen Hürden bei der Erstattungsfähigkeit der Antiallergika für gesetzlich versicherte AR-Patienten zu sehen. Licht am Ende des Tunnels könnte nun das neue Nasenspray Dymista® (Azelastinhydrochlorid und Fluticasonpropionat) bringen.
Mittel der Wahl: in Studien geprüft und voll erstattungsfähig
Dymista wurde in vier doppelblinden, placebokontrollierten Phase-III-Studien [6,7] und in einer offenen Langzeit-Sicherheitsstudie [8] mit annähernd 5.000 Teilnehmern untersucht. Das Design der Studien sah eine siebentägige Placebophase vor, auf die eine 14-tägige Verumphase folgte. Während dieser erhielten die Patienten randomisiert MP29-02 (Studienbezeichnung von Dymista), Fluticason, Azelastin oder Placebo täglich als Nasenspray. In die Studien eingeschlossen waren Patienten, die seit zwei oder mehr Jahren an einer AR mit mittelschwerer bis schwerer Symptomatik litten und einen positiven Prick-Test für relevante Allergene aufwiesen. Der primäre Endpunkt wurde als die Veränderung der Summe der durchschnittlichen morgendlichen und abendlichen nasalen Symptome (reflective total nasal symptom score – rTNSS) im Vergleich zum Ausgangswert unter Berücksichtigung des Placeboeffektes definiert.
Schnelle Linderung der nasalen und okularen Symptome
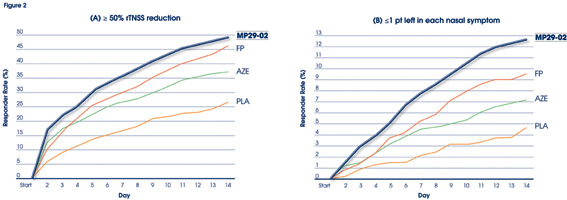
In jeder der Phase-III-Studien reduzierten die Verum-Substanzen den mittleren rTNSS stärker als Placebo. Dabei zeigte sich MP29-02 den beiden Einzelsubstanzen signifikant überlegen (p<0,001, s. Abb. 1). Zudem erreichten die Patienten mit Dymista bis zu drei Tage früher als unter Fluticason und bis zu fünf Tage früher als unter Azelastin eine 50%-ige Reduktion des rTNSS. Zum Studienende waren mehr Patienten mit dem neuen Präparat vollständig oder nahezu vollständig symptomfrei als unter den Einzelsubstanzen (s. Abb. 1). Auch die okularen Symptome konnten mit Dymista im Vergleich zu den Einzelsubstanzen deutlich reduziert werden. Bei vergleichbarem Nebenwirkungsprofil wie die Standardtherapeutika wurde Dymista insgesamt gut vertragen [8].
Dymista ist mehr als nur eine fixe Kombination. Bei Dymista handelt es sich um eine neuartige intranasale Therapie. Um die beiden Wirkstoffe Fluticason und Azelastin in eine Suspension zu bringen, bedurfte es einer neuen galenischen Aufbereitung. Die daraus resultierende bessere Wirkung wird deutlich, wenn die Ergebnisse der Zulassungsstudien [7] mit den Ergebnissen aus der Studie [8] gegen am Markt erhältliche Produkte verglichen werden.
Dymista gilt unter internationalen Experten bereits jetzt als Mittel der Wahl [7]). Jüngst wurde es von den Herausgebern des Journals of Allergy & Clinical Immunology als „bedeutender Fortschritt bei der Behandlung der Allergischen Rhinitis“ beschrieben. „Ich denke, „Dymista wird die Therapielandschaft der AR nachhaltig zum Positiven verändern“, kommentierte Klimek die Zulassungsstudien.
Referenzen
-
Bauchau V. et al. Eur Respir J 2004;24:758-764
-
Hellgren J et al. Allergy 2010;65(6): 776-783
-
Bousquet PJ et al. Int Arch Allergy Immunol 2012;160(4):393-400
-
Maurer M et al. Allergy 2007;62:1057-1063
-
Lamb CE et al. Curr Med Res Opin 2006;22(6):1203-10
-
Hampel FC et al. Ann Allergy Asthma Immunol 2010;105:168-173
-
Carr W et al. J Allergy Clin Immunol 2012;129:1282-1289
-
Price D et al. Allergy 2012;67(Suppl 96)336-337
Abbildung

Abb. 1 : Anteil (A) der Patienten mit einer Verbesserung der durchschnittlichen morgendlichen und abendlichen nasalen Symptome um 50% und (B) der Patienten mit einem Punktwert <= 1 für alle nasalen Symptome, jeweils pro Behandlungstag (modifiziert nach [7])
Über Dymista®
Dymista ist in Deutschland seit dem 18. März 2013 zugelassen zur Linderung der Symptome der
mittelschweren bis schweren saisonalen und perennialen Allergischen Rhinitis, wenn eine Monotherapie entweder mit einem intranasalen Antihistaminikum oder einem Glukokortikoid nicht als ausreichend erachtet wird.
Über MEDA
Meda AB ist ein führendes internationales Pharmaunternehmen, dessen Präparate weltweit in mehr als 120 Ländern erhältlich sind. Das Unternehmen wird in über 50 Ländern durch eigene Vertriebsstellen repräsentiert. Die Meda-Aktien sind unter dem "Large Cap" im Nasdaq OMX Nordic Stock Exchange in Stockholm gelistet.
-
Mehr Informationen finden Sie unter www.meda.se
Quelle: MEDA Pharma, 24.05.2013 (tB).