MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Therapieziele erreichen – praktisches Vorgehen bei PAH-Patienten entsprechend den aktuellen Leitlinien
Prof. Dr. med. Ralf Ewert
Wiesbaden (11. April 2010) – In den letzten Jahren wurden mehrfach die nicht medikamentösen und medikamentösen Ansätze bei der Behandlung von Patienten mit einer pulmonalen Hypertonie einer umfangreichen Bewertung unterzogen. Für eine Klasse dieser Patienten – nämlich mit pulmonal arterieller Hypertonie (PAH) – wurde vor Kurzem ein international akzeptierter Therapiealgorithmus unter Einbeziehung spezifischer medikamentöser Ansätze in aktualisierter Form verabschiedet. Diese Empfehlungen der European Society of Cardiology (ESC) und der European Respiratory Society (ERS) basieren auf den mittlerweile vorliegenden Daten einer Vielzahl randomisierter Studien und Beobachtungsstudien zu verschiedenen Patientengruppen aus der Klasse der PAH-Patienten.1, 2
Mit den heute zur Verfügung stehenden Behandlungsoptionen können das Überleben der Patienten sowie die körperliche Leistungsfähigkeit und die Befindlichkeit signifikant verbessert werden.3 Zugleich zeigen die Daten jedoch, dass auch heute keine Heilung der Patienten möglich ist. Unter Ausschöpfung aller supportiver Maßnahmen und einer dauerhaften Mono- bzw. zunehmend Kombinationstherapie zeigt sich ein Überleben von etwa 80 Prozent nach 3 Jahren.1, 2
Wie kennen heute eine Reihe prognostisch relevanter Faktoren, welche zur Definition von sogenannten „Zielkriterien“ für die Therapie herangezogen werden. Diese Zielkriterien unter optimierter Therapie sind: das Erreichen der NYHA-Klasse I/II bzw. die Stabilisierung in der NYHA-Klasse II, das Fehlen von Synkopen, eines Rechtsherzversagens oder progredienten Krankheitsverlaufes sowie eine angemessene kardiopulmonale Belastbarkeit. Für diese Parameter existieren u. a. laborchemische, hämodynamische, echokardiographische und klinische Befunde, die eine Unterscheidung von „guter“ bzw. „schlechter“ Prognose erlauben.1 Die Höhe des pulmonal arteriellen Drucks, unabhängig davon, ob echokardiographisch abgeschätzt oder invasiv ermittelt, spielt für die prognostische Beurteilung von Patienten mit PAH und für therapeutische Entscheidungen praktisch keine Rolle. Dem Behandler stehen somit verschiedene Kriterien zur Verfügung, die das individuelle therapeutische Vorgehen mit statistisch gesicherten Daten unterstützen.
Bei Akzeptanz dieser Zielkriterien stellen sich u. a. folgende offene Fragen:
-
Existieren besonders wichtige Kriterien, welche die Prognose mehr beeinflussen als andere?
-
Wie häufig sollen diese Parameter bei den Patienten erfasst werden?
-
In welchen Zeiträumen sollten die Ziele erreicht werden?
Bei PAH der NYHA-Klasse II oder III empfehlen die aktuellen Leitlinien zunächst eine Monotherapie. In Deutschland wird nach Einleitung einer supportiven Behandlung häufig eine orale Monotherapie mit einem PDE-Hemmer bzw. Endothelin-Rezeptor-Antagonisten (ERA) begonnen. Je nach klinischer Situation sollte im weiteren Verlauf in etwa 3- bis 6‑monatigen Abständen überprüft werden, ob die Therapieziele erreicht wurden. Sollte dies nicht der Fall sein, wird eine Therapieerweiterung im Sinne einer Kombinationstherapie empfohlen. Bei PAH-Patienten, die sich im Stadium NYHA-Klasse IV vorstellen, kann eine Kombinationstherapie auch primär erwogen werden.
Die meisten der bisher durchgeführten Studien zur PAH-Therapie waren mit einer Monotherapie angelegt, wobei im Zeitverlauf ein Teil der Patienten dann eine Kombinationstherapie erhielt. Es ist häufig aus den Originaldaten nicht zu erheben, in welchem Anteil die Patienten bestimmte Zielkriterien erreichten. Eine monozentrische Beobachtung zeigte die Notwendigkeit einer 2‑fach-Therapie für 43 Prozent und einer 3‑fach-Therapie für weitere 16 Prozent der Patienten, um vordefinierte Zielkriterien zu erreichen.8 Vor diesem Hintergrund gewinnen Kombinationsstudien mehr an Bedeutung; diese liegen bereits vor in randomisierter, plazebokontrollierter Form für die Kombination intravenöses Epoprostenol mit Bosentan (BREATHE‑2)10, Bosentan mit inhalativem Iloprost (STEP-Studie, COMBI-Studie)11, 12 sowie intravenöses Epoprostenol mit Sildenafil (PACES-Studie).13
Diese Daten werden durch eine Vielzahl von unkontrollierten Beobachtungen verschiedener Kombinationen bei unterschiedlichen Patientengruppen ergänzt. Dabei sind vielfältige Kombinationen durch erste vorliegende Ergebnisse als sicher und wirksam bewertet.
Zudem existieren erste Hinweise darauf, dass bereits eine frühere medikamentöse Kombinationsbehandlung als sinnvoll angesehen werden kann. So zeigte sich bei 25 Patienten (IPAH und PAH assoziiert mit Kollagenosen) mit Bosentan, welche bei klinischer Verschlechterung zusätzlich Sildenafil erhielten, eine ausreichende Stabilisierung für die IPAH-Patienten.14 In der ausschließlich mit Patienten in der NYHA-Klasse‑II durchgeführten EARLY-Studie konnte auch für 15 Prozent der Patienten mit einer Kombination von Bosentan und Sildenafil eine Verbesserung der Gehstrecke nach 6 Monaten gezeigt werden. Somit konnte erstmalig auch ein Vorteil hinsichtlich der kombinierten Behandlung für Patienten in einem frühen Krankheitsstadium belegt werden.15
Vor dem Hintergrund der mittlerweile vorliegenden Zielkriterien werden zukünftige Studien zeigen müssen, inwieweit wir in der Lage sind, diese für einen relevanten Anteil von Patienten zu erreichen.
FAZIT
Die aktuellen Leitlinien zur Diagnostik und Therapie der pulmonal arteriellen Hypertonie legen zum ersten Mal Therapieziele wie zum Beispiel Besserung und Stabilisierung der NYHA-Klasse mindestens auf NYHA-Klasse II zur Steuerung der Therapie fest.
In etwa 3- bis 6‑monatigen Abständen soll die Zielerreichung überprüft werden. Sollten die Therapieziele nicht erreicht werden, wird eine Therapieerweiterung im Sinne einer Kombinationstherapie empfohlen. Der chronische und rasch progrediente Verlauf der PAH ist die Rationale für eine Kombinationstherapie zum Erreichen dieses Therapieziels.
Kontrollierte Langzeitstudien zu Kombinationstherapien bei PAH (wie zum Beispiel COMPASS‑2 und COMPASS‑3) werden durchgeführt, um die Wirksamkeit und die Erreichbarkeit der Therapieziele zu zeigen.
Literatur
-
Galiè N et al. Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Respir J 2009; 34: 1219–1263.
-
Galiè N et al. Guidelines for the diagnosis and treatment of pulmonary hypertension: The Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS), endorsed by the International Society of Heart and Lung Transplantation (ISHLT). Eur Heart J 2009; 30: 2493–2537.
-
Galiè N et al. A meta-analysis of randomized controlled trials in pulmonary arterial hypertension. Eur Heart J 2009; 30: 394–403.
-
D’Alonzo GE et al. Survival in Patients with Primary Pulmonary Hypertension. Results from a National Prospective Registry. Ann Intern Med 1991; 115: 343–349.
-
Barst RJ et al. A comparison of continuous intravenous Epoprostenol (prostacyclin) with conventional therapy for primary pulmonary hypertension. N Engl J Med 1996; 334: 296–301.
-
Fachinformation Tracleer®
-
McLaughlin VV et al. Survival with first-line bosentan in patients with primary pulmonary hypertension. Eur Respir J 2005; 25: 244–249.
-
Hoeper MM et al. Goal-oriented treatment and combination therapy for pulmonary arterial hypertension. Eur Respir J 2005; 26: 858–863.
-
Provencher S et al. Longterm outcome with first-line bosentan therapy in idiopathic pulmonary arterial hypertension Eur Heart J 2006; 27: 589–595.
-
Humbert M et al. Combination of bosentan with epoprostenol in pulmonary arterial hypertension: BREATHE‑2. Eur Respir J 2004; 24: 353–359.
-
McLaughlin VV et al. Randomized study of adding inhaled iloprost to existing bosentan in pulmonary arterial hypertension. Am J Respir Crit Care Med 2006; 174: 1257–1263.
-
Hoeper M et al. Combining inhaled iloprost with bosentan in patients with idiopathic pulmonary arterial hypertension. Eur Respir J 2006; 28: 691–694.
-
Simonneau G et al. Addition of sildenafil to long-term intravenous epoprostenol therapy in patients with pulmonary arterial hypertension: a randomized trial. Ann Intern Med. 2008; 149: 521–530.
-
Mathai SC et al. Addition of sildenafil to bosentan monotherapy in pulmonary arterial hypertension. Eur Respir J 2007; 29: 469–475.
-
Galiè N et al. Treatment of patients with mildly symptomatic pulmonary arterial hypertension with bosentan (EARLY study): a double-blind, randomised controlled trial. Lancet 2008; 371: 2093–2100.
-
Grünig E et al. Acute hemodynamic effects of single-dose sildenafil when added to established bosentan therapy in patients with pulmonary arterial hypertension: results of the COMPASS‑1 study. J Clin Pharm 2009; 49: 1343–1352.
Abbildungen

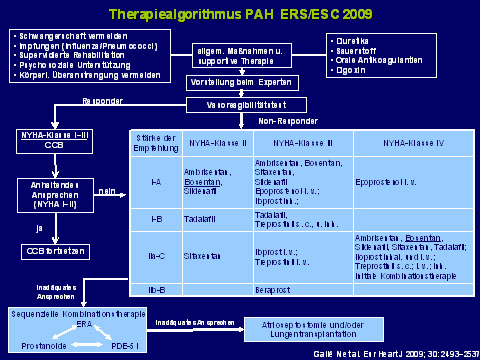
Abb. 1: Therapiealgorithmus PAH ERS/ESC 2009.

Abb. 2: Therapieziel bei PAH: NYHA-Klasse II.

Abb. 3: Empfohlene Verlaufsuntersuchungen bei Patienten mit PAH.

Abb. 4: Prognostische Parameter bei PAH.
Autor
Prof. Dr. med. Ralf Ewert
Klinik und Poliklinik für Innere Medizin
Universitätsklinikum der Ernst-Moritz-Arndt-Universität Greifswald
Quelle: Satellitensymposium der Firma Actelion zum Thema “Pulmonal arterielle Hypertonie und digitale Ulzerationen: zwei Diagnosen – eine Therapie” am 11.04.2010 in Wiesbaden (DGIM Kongress 2010) (Cramer-Gesundheits-Consulting) (tB).