MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Therapie des multiplen Myeloms mit Bortezomib
Verbessertes Ansprechen und längeres Überleben
Neuss (25. September 2012) – Bortezomib ist der erste Vertreter eines innovativen antitumoralen Wirkprinzips, der Proteasom-Inhibition. Klinische Studien zeigen, dass Bortezomib die Zeit bis zum Fortschreiten der Erkrankung bei Patienten mit multiplem Myelom sowohl in der Erstlinien- als auch in der Rezidivtherapie deutlich verlängern kann.(1,2,3) Besonders hervorzuheben ist der nachhaltige Überlebensvorteil, der durch eine Primärtherapie mit Bortezomib erzielt werden kann. Die Therapie mit dem Proteasom-Inhibitor bietet Patienten darüber hinaus lange Behandlungspausen und damit eine Steigerung der Lebensqualität.(4)
Bortezomib ist sowohl für die Primär- als auch für die Rezidivtherapie des multiplen Myeloms zugelassen. In der Primärtherapie ist es indiziert in Kombination mit Melphalan und Prednison für die Behandlung von erwachsenen Patienten, die für eine Hochdosis-Chemotherapie mit Knochenmarktransplantation nicht geeignet sind. Als Monotherapie ist es indiziert für die Behandlung von erwachsenen Patienten mit progressivem, multiplem Myelom, die mindestens eine vorangehende Therapie durchlaufen und die sich bereits einer Knochenmarktransplantation unterzogen haben oder die für eine Knochenmarktransplantation nicht geeignet sind. Bortezomib kann sowohl intravenös als auch subkutan verabreicht werden. Die subkutane Gabe bietet gegenüber der intravenösen Verabreichung eine bessere Verträglichkeit bei bewährter Wirksamkeit.(5)
VMP in der Primärtherapie: Überlebensvorteil gegenüber MP
Ein primäres Ziel der Myelom-Therapie ist eine maximale Lebensverlängerung. Die Überlebensrate war Endpunkt mehrerer klinischer Studien mit Bortezomib. Die aktuelle 5-Jahres-Nachbeobachtung der Zulassungsstudie VISTA bestätigte, dass Patienten, die eine Kombination aus Bortezomib, Melphalan und Prednison (VMP) in der Primärtherapie erhalten hatten, einen deutlichen Überlebensvorteil gegenüber den Patienten aufwiesen, die nur Melphalan und Prednison (MP) erhalten hatten. Das mediane Gesamtüberleben nach fünf Jahren Nachbeobachtung betrug im VMP-Regime 56,4 Monate gegenüber 43,1 Monate im MP-Arm. Dieser Unterschied ist umso relevanter, da die Hälfte der MP-Patienten nachfolgend noch eine Therapie mit Bortezomib erhalten hatten.(6) Der Überlebensvorteil einer primären Behandlung mit Bortezomib kann also durch eine spätere Gabe nicht mehr aufgeholt werden.
Bedeutung der Qualität des Ansprechens
Die Qualität des Ansprechens einer Tumortherapie ist ein entscheidender prognostischer Faktor für eine längere Progressionsfreiheit und ein längeres Gesamtüberleben.(7) Unter VMP wurden in der VISTA-Studie signifikant bessere Ansprechraten (p < 0,001) und eine längere Remissionsdauer als unter MP festgestellt. Von den mit VMP behandelten Patienten erreichten 30 % eine komplette Remission, unter MP waren es nur 4 %. Dabei wurde die komplette Remission unter VMP nach median 4,2 Monaten, unter MP nach median 5,3 Monaten erreicht. Gleichzeitig folgte der kompletten Remission unter VMP eine deutlich längere Remissionsdauer von median 24 Monaten gegenüber median 12,8 Monaten unter MP.(3)
Eine längere Therapie-freie Zeit (TFZ) bedeutet für Patienten mit multiplen Myelom einen deutlichen Gewinn an Lebensqualität. Die Primärtherapie mit VMP bietet Patienten im Vergleich zu MP nicht nur eine Verlängerung der Zeit bis zur Tumorprogression von 16,6 auf 24 Monate(6), sondern vor allem eine doppelt so lange TFZ (VMP: 16,6 Monate, MP: 8,3 Monate).(4) 42,7 % der mit VMP behandelten Patienten hatte eine TFZ von mehr als zwei Jahren.(6) VMP-Patienten mit einer kompletten Remission erfuhren eine verlängerte TFZ von median 29 Monaten gegenüber median 13,9 Monaten bei Patienten mit einer partiellen Remission.(8)
Eine möglichst hohe Zahl von Behandlungszyklen (bis zu neun Zyklen VMP gemäß Velcade®-Fachinformation(5)) erhöht die Chance auf eine CR. Denn 28 % aller kompletten Remissionen unter VMP wurden nach der 24. Behandlungswoche erzielt. Der Zeitpunkt des Ansprechens hatte dabei keine Auswirkungen auf die Dauer der Remissionen.(8)
Retreatment mit Bortezomib
Die Therapieentscheidung insbesondere bei der Primärbehandlung des multiplen Myeloms hängt auch davon ab, welche Therapieoptionen für die Rezidivbehandlung offen bleiben. Patienten der VISTA-Studie, die erfolgreich in der Primärtherapie mit VMP behandelt worden sind, sprachen zu 47,0 % im Retreatment wieder auf Bortezomib an, wobei 6,0 % der Patienten eine komplette Remission erzielten.(6)
Eine Studie mit stark vorbehandelten Patienten zeigte, dass bei Patienten, die unter einer vorherigen Rezidivtherapie mit Bortezomib eine CR erreicht hatten, die Ansprechrate im Retreatment sogar bei 75 % lag.(9)
Nebenwirkungsprofil von Bortezomib
Die Sicherheit und Verträglichkeit von Bortezomib sowohl als Mono- als auch als Kombinationstherapie mit MP wurden in mehreren klinischen Studien untersucht. Zu den häufigsten Nebenwirkungen einer Bortezomib-Therapie gehören z.B. Erkrankungen des Blutes (Neutropenie, Thrombozytopenie, Anämie), des Gastrointestinaltraktes (Übelkeit, Diarrhö, Erbrechen, Obstipation), des Nervensystems (periphere Neuropathie, Neuralgie, Parästhesie) sowie Symptome, die das Allgemeinempfinden betreffen (Müdigkeit, Kraftlosigkeit, Fieber).(5) 79 % der peripheren Neuropathien unter VMP besserten sich oder waren komplett reversibel (innerhalb median 1,9 Monaten), innerhalb von 5,7 Monaten bildeten sich 60 % der peripheren Neuropathien vollständig zurück.(6)
Durch die subkutane Gabe von Bortezomib kann die Rate der Nebenwirkungen deutlich gesenkt werden, ohne Einbußen in der Wirksamkeit hinnehmen zu müssen. Insgesamt reduzierte sich der Anteil der Patienten mit ≥ Grad 3 Nebenwirkungen bei subkutaner Darreichung auf 57 % (vs. 70 % bei intravenöser Darreichung). Die Rate aller peripheren Neuropathien sank durch die subkutane Gabe auf 38 % gegenüber 53 % bei intravenöser Gabe. ≥ Grad 3 priphere Neuropathien traten unter Bortezomib s.c. nur noch bei 6 % der Patienten auf (vs. 16 % unter Bortezomib i.v.). Auch der Anteil der Therapieabbrüche aufgrund schwerer Nebenwirkungen konnte reduziert werden (22 % vs. 27 %).(10)
Nutzen der Bortezomib-Therapie für ältere Patienten
Das mediane Alter der Patienten in der VISTA-Studie lag bei 71 Jahren. 30 % waren älter als 75 Jahre.(2) Eine Subgruppenanalyse dieser Patienten zeigte, dass Bortezomib auch für Patienten ab 75 Jahren eine gut wirksame und gut verträgliche Option darstellt. 26 % der Patienten über 75 Jahren im VMP-Arm erreichten eine komplette Remission, unter MP nur 3 %. Auch hinsichtlich des Gesamtüberlebens zeigte sich der Nutzen einer Behandlung mit Bortezomib in dieser Patientengruppe: Das mediane Gesamtüberleben lag unter VMP deutlich höher als unter MP (50,7 vs. 32,9 Monate)(4). Der Wert für die mediane Zeit bis zur Progression wurde unter VMP noch nicht erreicht, während er im MP-Arm bei 16,4 Monaten lag. Die Nebenwirkungen der Behandlung mit VMP waren bei Patienten über 75 Jahre mit denen jüngerer Patienten vergleichbar.(11)
Positive Wirkung auf den Knochenstoffwechsel
Der krankheitsbedingte gestörte Knochenstoffwechsel bei Menschen mit multiplem Myelom führt häufig zu Knochenschmerzen bis hin zu pathologischen Frakturen. Auch kann es durch den gesteigerten Knochenabbau zu Hyperkalzämie mit entsprechenden Symptomen kommen.(12) Der Proteasom-Inhibitor Bortezomib kann den gestörten Knochenstoffwechsel regulieren, indem er sowohl die Aktivität knochenabbauender Osteoklasten hemmt(13,14,15) als auch die Differenzierung und Aktivität der knochenaufbauenden Osteoblasten steigert.(16,17,18) Histomorphologische Analysen zeigen, dass im Ergebnis sowohl das Knochenvolumen als auch die trabekuläre Vernetzung unter Bortezomib zunehmen können.(16)
Einsatz von Bortezomib bei Niereninsuffizienz
Niereninsuffizienz liegt bei rund 16 % aller neu diagnostizierten Myelompatienten vor. Diese Patienten haben im Allgemeinen eine schlechtere Prognose und sind oft schwierig zu behandeln. Hinzu kommt, dass die Niereninsuffizienz eine häufige Myelom assoziierte Komplikation darstellt.(19) Bortezomib kann unter engmaschiger Beobachtung sowohl bei Patienten mit eingeschränkter Nierenfunktion als auch bei Patienten mit terminaler Niereninsuffizienz eingesetzt werden.(7) Studien zeigen die gute Verträglichkeit und hohe Wirksamkeit des Wirkstoffs bei Patienten mit Nierenfunktionsstörungen. In der VISTA-Studie erreichten 31 % der niereninsuffizienten Patienten (Baseline CrCl < 50 ml/min) unter VMP eine CR. Von besonderer Bedeutung ist, dass unter VMP die Erholung der Nierenfunktion (entspricht einer Verbesserung der Werte auf GFR ≥ 60 ml/min unter Behandlung) höher war als unter MP (44 % vs. 34 % bei Patienten mit Kreatinin-Clearance < 50 ml/min).(20)
Anmerkungen
-
Richardson PG et al., Cancer 2006;106:1316-1319
-
Richardson PG et al., N Engl J Med 2005;352:2487-2498
-
San Miguel JF et al., N Engl J Med 2008;359:906-917
-
San Miguel JF et al., ASH 2011;San Diego;Abstract #476
-
Aktuelle Velcade® Fachinformation
-
Mateos M-V et al., J Clin Oncol 2010;28:2259-2266
-
Chanan-Khan AA, Giralt S, J Clin Oncol 2010;28:2612-2624
-
Harrousseau JL et al., Blood 2010;116:3743-3750
-
Hrusovsky I et al., Oncology 2010;79:247-251
-
Moreau P et al., Lancet oncol 2011;12(5):431-440
-
Kropff M et al., XII International Myeloma Workshop 2009;
Poster #084 -
DGHO-Leitlinie Multiples Myelom, Stand: Juli 2010: http://www.dgho.de/onkopedia/Multiples%20Myelom, Zugriff am 25.01.2011
-
von Metzler I et al., Leukemia 2007;21:2025-2034
-
Terpos E et al., Br J Haematol 2006;135(5):688-692
-
Boissy P et al., Blood 2006;108:1000a.Abstract 2508
-
Pennisi A et al., Am J Hematol 2008;published online: www.interscience.wiley.com DOI:10.1002/ajh.21310, Zugriff am 25.01.2011
-
Giuliani D at al., Blood 2007;110:334-338
-
Zangari M et al., Br J Haematol 2005;131(1):71.73
-
Knauff W et al., DGHO 2009 Abstract P489 Poster
-
Dimopoulos M et al., J Clin Oncol 2009;27:6086-6093
Abbildungen

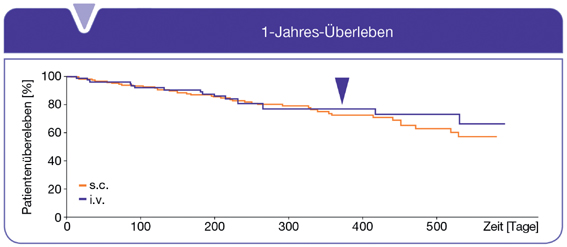
Abb. 1: Die 1-Jahres-Überlebensrate ergab mit 72,6 % bei subkutaner und 76,7 % bei der intravenösen Anwendung von Velcade® keinen signifikanten Unterschied. © Janssen-Cilag GmbH
Quelle: modifiziert nach Moreau P et al., Lancet Oncol 2011;431–440

Abb. 2: Das mediane Gesamtüberleben nach fünf Jahren Nachbeobachtung betrug unter der Therapie mit Velcade® in Kombination mit Melphalan und Prednison (VMP) 56,4 Monate vs. 43,1 Monaten unter Melphalan und Prednison alleine (p = 0,0004). © Janssen-Cilag GmbH
Quelle: modifiziert nach San Miguel JF et al., ASH 2011; San Diego;Abstract #476

Abb. 3: Patienten, die mit einer kompletten Remission (CR) auf die Behandlung mit Velcade® in Kombination mit Melphalan und Prednison (VMP) angesprochen hatten, erreichten eine besonders lange Zeit bis zur nächsten Therapie (TNT) und Therapie-freie Zeit (TFZ). © Janssen-Cilag GmbH
Quelle: erstellt nach Harousseau JL et al., Blood 2010;116(19):3743-3750

Abb. 4: Die Behandlung mit Velcade® in Kombination mit Melphalan und Prednison (VMP) kann eine lange Zeit bis zur nächsten Therapie (TNT) sowie eine lange Therapie-freie Zeit (TFZ) ermöglichen. © Janssen-Cilag GmbH
Quelle: erstellt nach San Miguel JF et al., N Engl J Med 2008; 359:906-917 (1); San Miguel JF et al., ASH 2011; San Diego;Abstract #476

Abb. 5: Die Primärtherapie mit Velcade® in Kombination mit Melphalan und Prednison (VMP) führte zu einer signifikant (p < 0,001) höheren Rate kompletter Remissionen (CR) und einer längeren Remissionsdauer. © Janssen-Cilag GmbH
Quelle: erstellt nach San Miguel JF et al., N Engl J Med 2008; 359:906-917
Download
-
Fact Sheet multiples Myelom:
 Fact Sheet_Multiples_Myelom.pdf (235.33 KB)
Fact Sheet_Multiples_Myelom.pdf (235.33 KB)
Quelle: Janssen-Cilag, 25. 09.2012 (tB).