MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Typische CLL-Patienten
Progressionsfreies Überleben mit Gazyvaro (Obinutuzumab) nahezu verdoppelt
Hamburg (24. Juni 2015) – In der Zulassungsstudie CLL11 hatte der Typ-II-Anti-CD20-Antikörper Gazyvaro® (Obinutuzumab) in Kombination mit Chlorambucil seine deutliche Überlegenheit gegenüber der Chemoimmuntherapie mit dem bisherigen Therapiestandard Mab-Thera® (Rituximab) und auch der Chlorambucil-Monotherapie bewiesen.1 Ein Update der von Roche in Zusammenarbeit mit der Deutschen CLL-Studiengruppe (DCLLSG) durchgeführten Studie zeigt nun nochmals eine Verbesserung des progressionsfreien Überlebens (PFS) sowie eine deutliche Verlängerung der behandlungsfreien Zeit um zehn Monate auf über dreieinhalb Jahre.2 Damit bestätigt Obinutuzumab erneut seinen Stellenwert als zentraler Baustein der Erstlinien-Therapie typischer Patienten mit chronischer lymphatischer Leukämie (CLL).
Die Verlängerung des Gesamtüberlebens (OS) gegenüber der Chlorambucil-Monotherapie sowie die hohe Remissionsqualität haben Gazyvaro im Praxisalltag bereits als neuen Therapiestandard etabliert.1 Dr. Volkmar Böhme, niedergelassener Hämatologe und internistischer Onkologe in der Hamburger Praxis und Tagesklinik Onkologie Lerchenfeld, erläutert deshalb im Rahmen eines Pressegespräches der Roche Pharma AG: „Mit Gazyvaro haben wir bei der Erstlinien-Therapie typischer CLL-Patienten einen echten Fortschritt erreicht. Das progressionsfreie Überleben verlängert sich im Vergleich zu MabThera um mehr als ein Jahr. Das ist ein sehr guter Erfolg, da dadurch für die Patienten Folgetherapien weit hinausgezögert werden können.“
Wie außergewöhnlich die mit Obinutuzumab erreichte Qualität von Remissionen ist, zeigt sich auch an deren „Tiefe“: In der CLL11-Studie war der Anteil von Patienten mit nicht mehr nachweisbarer minimaler Resterkrankung (MRD) in der Obinutuzumab-Chlorambucil-Gruppe im Vergleich zu Rituximab-Chlorambucil mehr als verzehnfacht (37,7% vs. 3,3%). Dieses Resultat gewinnt vor dem Hintergrund einer beim ASH-Kongress 2014 vorgestellten kombinierten Analyse der DCLLSG-Studien CLL8 und CLL10 noch deutlich an Bedeutung. Dort erwies sich der MRD-Status im peripheren Blut als starker und unabhängiger Prognosefaktor für längeres PFS und war in der CLL8-Studie sogar prädiktiv für eine längere Gesamtüberlebensdauer.3
Update der CLL11-Studie: Signifikanter Therapiefortschritt
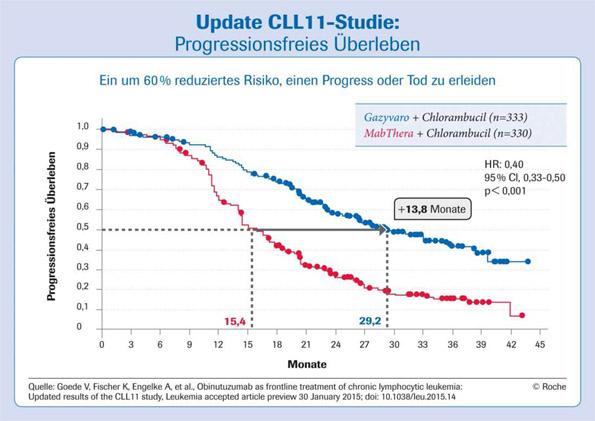
Das jüngst publizierte Update zur CLL11-Studie, in das Daten bis zum April 2014 mit eingingen, unterstreicht die bereits in der initialen Auswertung erkennbare deutliche Überlegenheit des Gazyvaro-Regimes.2 Unter der Kombination aus Obinutuzumab und Chlorambucil hatte sich die progressionsfreie Überlebenszeit gegenüber den mit Rituximab und Chlorambucil behandelten Patienten von 15,4 auf 29,2 Monate nahezu verdoppelt (Hazard Ratio 0,40; 95%- Konfidenzintervall 0,33–0,50; p < 0,001; s. Infografik). Außerdem konnte mit der Obinutuzumab-Kombination eine signifikante Verlängerung des OS im Vergleich zur Chlorambucil-Monotherapie erzielt werden (HR 0,47; 95%-KI 0,29–0,76; p = 0,0014). Der Unterschied beim OS hatte im Vergleich der beiden Antikörper-Arme noch keine statistische Signifikanz erreicht. Hierfür ist ein noch längerer Beobachtungszeitraum erforderlich.

Grafik: Mit Gazyvaro + Chlorambucil signifikante Verbesserung des progressionsfreien Überlebens auf über 29 Monate.2
Neben dem PFS verlängerte Obinutuzumab auch die behandlungsfreie Zeit zwischen den einzelnen Therapieintervallen. Im mit Obinutuzumab und Chlorambucil behandelten Arm lag dieser Zeitraum bei 42,7 Monaten gegenüber 32,7 Monaten unter Rituximab plus Chlorambucil (HR 0,54; 95%-KI 0,040–0,73; p < 0,001).
Gutes Sicherheitsprofil
Der Typ-II-Antikörper war gut verträglich. Die häufigsten Nebenwirkungen waren Infusions-assoziierte Reaktionen (IAR), die allerdings überwiegend während der ersten Infusion auftraten und meist gut behandelbar waren. Bei den nachfolgenden Infusionen gingen Häufigkeit und Schweregrad deutlich zurück. Ursache dieser ausgeprägten Reaktionen ist vermutlich die – durchaus erwünschte – schnelle und effektive Abtötung der malignen B-Zellen durch Obinutuzumab. Dabei werden Zytokine freigesetzt, die für das häufige Auftreten der IARs während der ersten Infusion verantwortlich sind.
Literaturverweise
-
Goede V et al. Obinutuzumab plus chlorambucil in patients with CLL and coexisting conditions. N Engl J Med 2014; 370: 1101-10.
-
Goede V, Fischer K, Engelke A, et al. Obinutuzumab as frontline treatment of chronic lymphocytic leukemia: Updated results of the CLL11 study, Leukemia accepted article preview 30 January 2015; doi: 10.1038/leu.2015.14.
-
Kovacs G et al. Value of minimal residual disease (MRD) negative status at response evaluation in chronic lymphocytic leukemia (CLL): Combined analysis of two phase III studies of the German CLL Study Group (GCLLSG). Blood 2014; 124(21): ASH 2014, Abstract #23.
Über Roche
Roche mit Hauptsitz in Basel, Schweiz, ist eines der führenden Unternehmen im forschungsorientierten Gesundheitswesen. Es vereint die Stärken der beiden Geschäftsbereiche Pharma und Diagnostics und entwickelt als weltweit größtes Biotech-Unternehmen differenzierte Medikamente für die Onkologie, Immunologie, Infektionskrankheiten, Augenheilkunde und Neurowissenschaften. Roche ist auch der weltweit bedeutendste Anbieter von Produkten der In-vitro-Diagnostik und gewebebasierten Krebstests und ein Pionier im Diabetesmanagement. Medikamente und Diagnostika, welche die Gesundheit, die Lebensqualität und die Überlebenschancen von Patienten entscheidend verbessern, sind Ziel der Personalisierten Medizin, eines zentralen strategischen Ansatzes von Roche. Seit der Gründung des Unternehmens im Jahr 1896 hat Roche über einen Zeitraum von mehr als hundert Jahren wichtige Beiträge zur Gesundheit in der Welt geleistet. Auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation stehen 28 von Roche entwickelte Medikamente, darunter lebensrettende Antibiotika, Malariamittel und Chemotherapeutika.
Die Roche-Gruppe beschäftigte 2014 weltweit über 88 500 Mitarbeitende, investierte 8,9 Milliarden Schweizer Franken in Forschung und Entwicklung und erzielte einen Umsatz von 47,5 Milliarden Schweizer Franken. Genentech in den USA gehört vollständig zur Roche-Gruppe. Roche ist Mehrheitsaktionär von Chugai Pharmaceutical, Japan.
Weitere Informationen finden Sie unter www.roche.com
Roche Pharma AG, Deutschland
Die Roche Pharma AG in Grenzach-Wyhlen beschäftigt über 1.200 Mitarbeiterinnen und Mitarbeiter. Von hier aus werden alle zulassungsrelevanten Studien für Deutschland koordiniert. Darüber hinaus werden auch Studien für bereits auf dem Markt befindliche Produkte durchgeführt. Von Grenzach-Wyhlen aus erfolgen zudem zentrale Elemente der technischen Qualitätssicherung für den gesamten europäischen Raum. Außerdem ist die Roche Pharma AG für das Marketing und den Vertrieb verschreibungspflichtiger Arzneimittel auf dem gesamten deutschen Markt zuständig.
Weitere Informationen zur Roche Pharma AG finden Sie unter www.roche.de
Quelle: Roche Pharma, 24.06.2015 (tB).