PFLEGE
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
 „Wie erstarrt – Chancen durch frühe Therapie bei Parkinson“
„Wie erstarrt – Chancen durch frühe Therapie bei Parkinson“
Mit der Tiefen Hirnstimulation die Uhr anhalten
Düsseldorf (17. Mai 2014) – Der Mann steht mit dem Schlüssel in der Hand vor seiner Haustür. Seine Hand zittert so stark, dass er mit dem Schlüssel unmöglich das Schloss treffen kann – dies ist eine der typischen Erfahrungen der von der Parkinson-Erkrankung betroffenen Menschen. Es ist der verzweifelte Verlust der Kontrolle über einfachste Handgriffe wie Schuhe zubinden, Kaffee einschenken oder Mails schreiben. Parkinson ist keine typische Alterserkrankung: Rund 250.000 Menschen in Deutschland sind betroffen, ungefähr fünf Prozent von ihnen trifft die Diagnose vor dem Alter von 40 Jahren. „Viele Patienten haben nicht nur mit diesem plötzlichen Erstarren, dem Zittern und der verwaschenen Aussprache zu kämpfen, sondern ganz erheblich mit Vorurteilen“, weiß Dr. Michael Lorrain, Neurologe der Nervenarztpraxis Gerresheim. Über viele Betroffene wird auf der Arbeit getuschelt, oftmals werden sie des Alkoholmissbrauchs verdächtigt und immer kommt mit der schockierenden Diagnose das bewusste Miterleben der Krankheitssymptome. Vielfach helfen Medikamente, den Verlauf zu verlangsamen. Auch die Tiefe Hirnstimulation kann die Uhr anhalten. „Eine sehr bedeutende, aktuelle Studie zeigte, was wir Behandler bereits länger an unseren Patienten beobachtet haben: Die Tiefe Hirnstimulation kann in frühen Stadien der Erkrankung die sich verschlimmernden Symptome noch um Jahre hinauszögern“, berichtet Dr. Michael Lorrain. „Die EARLYSTIM-Studie hat zu einer Umkehr in der Behandlung von Parkinson geführt“, sagt er.
Das Parkinson-Syndrom, das auch vor Prominenten wie Papst Johannes Paul II., Schauspieler Michael J. Fox und Boxer Muhammad Ali nicht Halt macht, stützte sich bis vor kurzem auf Medikamente: In der ersten, der Honeymoon-Phase, klingen in der Regel die Symtome fast vollständig ab. Erst wenn diese ihre Wirkung verloren, hatten die Patienten die Möglichkeit, sich mit der Tiefen Hirnstimulation behandeln zu lassen. „Teilweise wurde jedoch – besonders bei Menschen mit kleinen Kindern in der Familie und Berufstätigen – diese Möglichkeit von den Patienten früher genutzt“, sagt Dr. Michael Lorrain. Erst eine große Studie an 251 Patienten in 17 Zentren in Europa belegte den Nutzen des Hirnschrittmachers auch in frühen Erkrankungsstadien wissenschaftlich.
Eine zentrale Rolle bei der Parkinsonkrankheit die Basalganglien des Hirns. Sie steuern die Muskelaktivität und die Koordination von Bewegungen. Die Aktivität dieser Basalganglien wird von Dopamin reguliert. Die Hirnzellen, die das Dopamin herstellen, sterben bei Parkinson ab. Der Dopaminmangel führt zu einer Überaktivität in den Basalganglien. Diese lässt sich mit Hilfe der Tiefen Hirnstimulation verhindern. Die typischen Symptome von Parkinson wie Zittern, unwillkürliche Bewegungen, das „Einfrieren“ und Muskelsteifheit verschwinden. Der Impulsgeber für die Elektroden im Kopf wird unter dem Schlüsselbein implantiert, ähnlich einem Herzschrittmacher. Die dünnen Elektroden setzen Neurochirurgen mit dreidimensionaler Bildgebung in den Thalamus ein. Dort senden sie elektrische Impulse, ähnlich wie die zuvor abgestorbenen Nervenzellen. „Wir betreuen viele Patienten mit einem Hirnschrittmacher in unserer Praxis. Alle von ihnen sind heilfroh über das neue Leben, das sie führen können und die meisten der berufstätigen Patienten arbeiten auch wieder“, fasst Dr. Lorrain zusammen.
HINTERGRUND
PARKINSON-KRANKHEIT
Parkinson ist eine unheilbare Krankheit, die ohne Vorwarnung auftritt und den Betroffenen langsam aber sicher ihre Eigenständigkeit nimmt. Symptome wie z.B. Zittern oder völlige Bewegungsunfähigkeit treten zunehmend auf und werden immer stärker. Schließlich können die Patienten kaum noch gehen, sprechen und alltägliche Dinge wie das all morgendliche Anziehen alleine verrichten oder normalen Beschäftigungen nachgehen1. Bei einigen Patienten mit Parkinson, kann die Unfähigkeit für sich selbst zu sorgen, zu einem Verlust von Selbstwertgefühl und zu Depressionen führen2,3. Auch Pflegende und Angehörige werden physisch und psychisch stark belastet. Viele müssen hilflos mit ansehen, wie sich der Zustand des Nahestehenden zunehmend verschlechtert.
Verursacht wird die neurologische Störung durch einen Verlust bzw. die Degeneration von Nervenzellen in einer tiefen Hirnregion (Substantia nigra), die den Botenstoff Dopamin produziert. Der Mangel an Dopamin verursacht Funktionsstörungen wichtiger Nervenzellen (Neurone), wodurch es bei den Patienten zu einem Kontrollverlust ihrer Bewegungen kommt. Die Parkinsonsche Krankheit ist wahrscheinlich die bekannteste neurologische Bewegungsstörung weltweit. Im vergangenen Jahrzehnt konnte man die tragischen Auswirkungen der Krankheit bei vielen berühmten Patienten wie Prinz Claus von Amsberg, den Schauspielern Raimund Harmstorf und Michael J. Fox, dem ehemaligen Box-Weltmeister Muhammad Ali und Papst Johannes Paul II beobachten.
Was sind die Ursachen und Fakten?
-
• Die meisten Menschen mit Parkinson leiden an so genanntem idiopathischen Parkinson-Syndrom (d.h. ohne spezifisch bekannte Ursache).
-
• Ein kleiner Anteil von Fällen kann jedoch auf bekannte genetische Faktoren zurückgeführt werden.
-
• Die Parkinsonsche Krankheit ist eine der häufigsten neurologischen Krankheiten. An ihr leiden weltweit schätzungsweise über vier Millionen Menschen – zuverlässige Prävalenzzahlen gibt es nicht4.
-
• In Deutschland sind ca. 250.000 Menschen von der Parkinsonschen Krankheit betroffen5.
-
• Männer und Frauen leiden gleichermaßen häufig unter Morbus Parkinson. Durchschnittlicher Krankheitsbeginn ist das 65. Lebensjahr6. Immer häufiger erkranken aber auch jüngere Menschen; acht bis zehn Prozent der Patienten sind zu Krankheitsbeginn nicht älter als 40 Jahre („early onset-Parkinson“).
-
• Die direkten Gesundheitsausgaben sowie die indirekten Kosten der Behinderungen und Produktivitätsverlust in Deutschland betragen ca. 20.000 Euro pro Patient und Jahr7.
Hauptsymptome sind:
-
• Rigor – Muskelsteifheit
-
• Bradykinese/Akinese – langsame/fehlende Bewegungen
-
• Tremor – unwillkürliches, regelmäßiges Zittern einer Extremität, des Kopfes oder des gesamten Körpers
-
• Haltungsinstabilität – Gang- und Gleichgewichtsstörungen. Zu den weiteren Symptomen zählen Angst, Muskelschmerzen, Schlafstörungen, Depressionen, Sprach- und Schluckstörungen sowie Gedächtnisverlust. Patienten mit Parkinson können extreme Schwankungen in der Bewegungskontrolle erfahren – von Zeiträumen mit nahezu normaler motorischer Funktion bis hin zu Episoden vollständiger Immobilität über eine Zeitspanne von ein paar Minuten oder sogar Stunden.
Welche Behandlungsmöglichkeiten gibt es?
Es ist wichtig zu erkennen, dass es derzeit keine Heilung von Parkinson gibt. Dennoch gibt es mehrere Behandlungsmöglichkeiten, welche die Symptome von Parkinson für viele Jahre wirksam bekämpfen können, was es den Patienten erlaubt, ein relativ normales Leben zu führen.
Medikamentöse Therapien:
Wenn die Symptome beginnen Einfluss auf den Lebensalltag der Patienten zu nehmen, können sie anfänglich mit kleinen Mengen oraler Anti-Parkinson-Medikamente (z. B. Dopamin-Agonisten, Levodopa, etc.) reduziert werden. Die Medikation soll die Menge an Dopamin erhöhen, welche das Gehirn erreicht oder die Hirnregionen stimulieren, wo das Dopamin normalerweise wirksam ist. Da der Zustand des Patienten fortschreitet, können höhere Dosen oder mehr als eine Art von Medikament notwendig werden, um die Symptome längerfristig zu kontrollieren. Dies kann jedoch mit einer Zunahme von Nebenwirkungen, wie Übelkeit, Erbrechen, Schwindel, Psychosen, Dyskinesien (Störung des Bewegungsablaufes) etc., verbunden sein. Schließlich kann es dazu kommen, dass Medikamente die Symptome eines Patienten nicht mehr wirksam kontrollieren oder sie zu beeinträchtigenden Nebenwirkungen führen können. Innerhalb von vier bis sechs Jahren nach Beginn der Behandlung mit Levodopa erfahren etwa 40 Prozent der Parkinson- Patienten motorische Dyskinesien, die ihre Lebensqualität beeinträchtigen8.
Tiefe Hirnstimulation (Deep Brain Stimulation, THS):
-
• Die Tiefe Hirnstimulation liefert elektrische Stimulation zur Modulation der Signale des Gehirns, welche die primären motorischen Symptome der Parkinson-Krankheit verursachen.
-
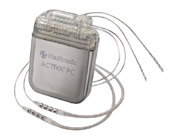
• Ein Neurostimulator wird chirurgisch unter der Haut im Brustbereich oder im Abdominalbereich implantiert und mit dünnen Elektroden in den Hirnregionen verbunden, die die Bewegungen kontrollieren. Dieses Stimulationssystem wird auch als „Hirnschrittmacher“ bezeichnet.
-
• Die Tiefe Hirnstimulation ist reversibel und auf die individuellen Bedürfnisse des Patienten einstellbar.
Die THS basiert auf einem chirurgisch implantierten Neurostimulator, ähnlich einem Herzschrittmacher, der die elektrische Stimulation von exakt festgelegten Strukturen im Gehirn übernimmt. Die Medtronic THS ist für dieBehandlung von Patienten, die trotz optimierter medikamentöser Therapie einschränkende Symptome der Parkinson-Erkrankung haben, zugelassen, sowie zur Behandlung früher Phasen der Erkrankung.
Das THS-System von Medtronic wird im Körper, üblicherweise im Brustbereich oder Bauch/Unterleib, von einem speziell ausgebildeten Neurochirurgen implantiert. Mithilfe hoch entwickelter Bilder des Patientengehirns wird der genau zu stimulierende Bereich bestimmt. Dünne, isolierte Drähte, Elektroden genannt, werden implantiert. Bei der Parkinson-Erkrankung erfolgt mit der THS eine gezielte Stimulation einer von zwei möglichen Hirnstrukturen, dem subthalamischen Nucleus oder dem Globus pallidus interna. Die Forschung zeigt, dass die Stimulation dieser Strukturen die Signale im Gehirn hemmt, welche die motorischen Symptome der Parkinson-Erkrankung wie Muskelsteifheit, verlangsamte Bewegung sowie Gang- oder Gleichgewichtsstörungen verursachen17,18. Diese Elektroden werden durch dehnbare Kabel mit dem Neurostimulator verbunden. Alle Komponenten des Hirnschrittmachers liegen unsichtbar unter der Haut.



Wirkungsweise der THS
Die Medtronic THS-Therapie bietet eine verbesserte Lebensqualität und etwa fünf zusätzliche Stunden "on" Zeit ohne Dyskinesien im Vergleich zu alleiniger optimaler medikamentöser Therapie9,10,11. Einige Patienten berichten von einer besseren Qualität des Schlafes und mehr Schlaf-Perioden mit der Tiefen Hirnstimulation12. Wenn Komplikationen bei der THS auftreten, sind sie in der Regel nicht schwerwiegend, und vorübergehend. Eine randomisierte (zufällig ausgewählte Personen) kontrollierte Studie mit THS Systemen von Medtronic weist eine Lösungsrate von 99 Prozent bezüglich der schwerwiegenden unerwünschten Ereignissen nach sechs Monaten auf13. THS wurde ausgiebig bei verschiedenen Erkrankungen untersucht. Die Medtronic THS Therapie hat ein gut etabliertes langfristiges Sicherheitsprofil, insbesondere bei jüngeren Patienten9,10,11,14.
Die Medtronic THS-Therapie kann den Patienten Vertrauen und Freiheit bieten mit der Gewissheit, dass die THSTherapie:
-
• Eine rund um die Uhr Stimulation bieten kann
-
• Auf ihre spezifischen Bedürfnisse programmiert und angepasst werden kann
-
• Vollständig implantierbar und in der Mehrzahl der Fälle nicht spürbar ist
-
• Reversibel ist und das System ausgeschaltet und bei Bedarf entfernt werden kann
Der richtige Patient soll eine Tiefe Hirnstimulation erhalten
-
• Die Medtronic THS Therapie wurde bis dato bei Parkinson Patienten im Spätstadium der Erkrankung mit einem maximalen Alter von etwa 70 bis 75 Jahren zur effektiven Behandlung der motorischen Symptome angewendet. Kandidaten waren Patienten mit Parkinson-Symptomen, welche mit Medikamenten nicht mehr kontrolliert werden konnten (z. B. ein Tremor, der sehr gut auf die THS anspricht) oder die Nebenwirkungen der Medikation nicht mehr tolerierbar waren.
-
• Eine neue Studie (EARLYSTIM) veröffentlicht im New England Journal of Medicine hat nun gezeigt, dass bereits Parkinson Patienten in einem sehr frühen Stadium der Erkrankung von der Medtronic THS Therapie profitieren können. Die Lebensqualität dieser Betroffenen wurde über einen Zeitraum von 24 Monaten signifikant verbessert, während es in der Kontrollgruppe unter alleiniger optimierter medikamentöser Therapie keine Veränderung gab16.
-
• Die Tiefe Hirnstimulation ist kein Allheilmittel und heilt nicht die Parkinson-Erkrankung. Wenn der Neurostimulator ausgeschaltet wird, kehren die Parkinson-Symptome meist zurück. Grundsätzlich variieren die individuellen Ergebnisse mit der THS-Therapie. Einige Patienten berichten von einer besseren Qualität des Schlafes und mehr Schlaf-Perioden mit der Tiefen Hirnstimulation12.
-
• Die Medtronic THS Therapie hält diese Verbesserungen der motorischen Symptome langfristig auch nach 5 Jahren aufrecht.15 Zudem erleichtert nicht-motorische Symptome, wie Schlafstörungen und Schmerzen aufgrund von Muskelkrämpfen (Dystonie) 19,20.
Die Wirksamkeit der THS-Therapie für die Parkinson-Krankheit
-
• Für motorische Fluktuationen und Dyskinesien erhielt STN-THS die höchste Empfehlung – Bewertungsgrad A – von der Movement Disorder Society-European Section (MDS-ES) in Zusammenarbeit mit der European Federation of Neurological Societies (EFNS). Im Vergleich dazu erhielten Duodopa- und Apomorphin-Pumpen den Empfehlungsgrad C.
-
• Die STN THS-Therapie ist verbunden mit einer durchschnittlichen Reduktion der Medikation um 32 bis 63 Prozent, abhängig von Studie und Zeitpunkt9,10,11,13,15.
Gesundheitlich-ökonomische Informationen
Zusätzlich zeigt eine aktuelle in Spanien durchgeführte Studie, dass die Tiefe Hirnstimulation einen geringeren Einsatz von Ressourcen im Gesundheitswesen bei fortgeschrittenem Parkinson erfordert. Für jeden Patienten, der jährlich mit Infusionstherapien (z.B. Apomorphin oder Levodopa/Carbidopa-Gel) behandelt wird, könnten stattdessen erhebliche Kosteneinsparungen durch den Einsatz der Tiefen Hirnstimulation realisiert werden21.
Weitere Informationen?
-
• Deutsche Gesellschaft für Neurologie, www.dgn.org
-
• Deutsche Parkinson Gesellschaft, http://www.kompetenznetz-parkinson.de
-
• The World Parkinson’s Disease Association – www.wpda.org
-
• The European Parkinson’s Disease Association – www.epda.eu.com
-
• Worldwide Education and Awareness for Movement Disorders (We Move) – http://www.wemove.org
Literaturverzeichnis
-
Schrag A, Dodel R, Spottke A, Bornschein B, Siebert U, Quinn NP. Rate of clinical progression in Parkinson’s disease. A prospective study. Mov Disord. 2007 15;22(7):938-45.
-
Parkinson’s Disease Society. Depression and Parkinson’s Information Sheet. Retrieved from http://www.parkinsons.org.uk/PDF/FS56_DepressionandParkinsons.pdf on 24 Jan 2012
-
Dissanayaka NN, Sellbach A, Silburn PA, O’Sullivan JD, Marsh R, Mellick GD.Factors associated with depression in Parkinson’s disease. J Affect Disord. 2011 Jul;132(1-2):82-8.
-
Kompetenznetz Parkinson www.kompetenznetz-parkinson.de
-
Kompetenznetz Parkinson www.kompetenznetz-parkinson.de, Deutsche Parkinson Vereinigung www.parkinson-vereinigung.de
-
Clarke C and Moore PA. Parkinson’s Disease. Clinical Evidence www.clinicalevidence.com/ceweb/conditions/nud/1203/1203_background.jsp
-
Dodel et al. Ökonomische Analyse des idiopathischen Parkinson-Syndroms – eine deskriptive prospektive 3-jährige Langzeitstudie.
-
Clarke C, Moore PA. Neurological disorders: Parkinson’s disease. Clinical Evidence. 2005; 13:1-4.
-
Deuschl G et al., A Randomized Trial of Deep‐Brain Stimulation for Parkinson’s Disease, NEJM, 355;9 2006
-
Weaver FM, et al., Bilateral THS vs. BMT for patients with advanced PD, JAMA 301(1):63‐73, 2009
-
Williams et al., Deep brain stimulation plus best medical therapy versus best medical therapy alone for advanced Parkinson’s disease (PD SURG trial): a randomised, open‐label trial, the Lancet Neurology, 9(6):581‐91,2010
-
Lyons KE and Pahwa R. Effects of bilateral subthalamic nucleus stimulation on sleep, daytime sleepiness, and early morning dystonia in patients with Parkinson’s disease. Journal or Neurosurgery. 2006; 104(4): 502-505
-
Weaver FM, et al., Bilateral THS vs. BMT for patients with advanced PD, JAMA 301(1):63‐73, 2009
-
Voges J, Hilker R, Botzel K, Kiening KL, Kloss M, Kupsch A. Thirty days complication rate following surgery performed for deep‐brain stimulation. Mov Disord 2007; 22(10):1486‐9.
-
Krack R, Batir A, Van Blercom N, at al. Five‐Year Follow‐up of Bilateral Stimulation of the Subthalamic Nucleus in Advanced Parkinson’s disease. N Engl J Med. 2003; 349: 1925‐34.
-
Deuschl, G. &al. Neurostimulation for Parkinson’s Disease with Early Motor Complications, 2013, New England Journal of Medicine: 610-622; 368
-
The Deep‐Brain Stimulation for Parkinson’s Disease Study Group. N Engl J Med. 2001;345:956‐963.
-
Esselink RA et al. Unilateral pallidotomy versus bilateral subthalamic nucleus stimulation in PD: a randomized trial. Neurology, 2004: 62(2): E6‐7
-
Deuschl G, Schade-Brittinger C, Krack P, Volkmann J, Schafer H, Botzel K et al. A randomized trial of deep brain stimulation for Parkinson’s disease. N Engl J Med 2006; 355:896-908.
-
Weaver F, Follett K, Stern M, Hur K, Harris C, Marks Jnr W et al. Bilateral deep brain stimulation vs best medical therapy for patients with advanced Parkinson’s disease. JAMA 2009; 301(1):63-73.
-
SCOPE Study; podium presentation at the XXXI Jornadas de Economía de la Salud, Mallorca May3rd‐6th 23 European Handbook of Neurological Management. European Handbook of Neurological Management: Volume 1, 2nd edition. Edited by N. E. Gilhus, M. P. Barnes and M. Brainin.© 2011 Blackwell Publishing Ltd. (Movement Disorder Society European Section (MDS‐ES) & European Federation of Neurological Societies (EFNS).
Quelle: Medtronic, 17.05.2014 (tB).