HAUPTMENÜ
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Dreifachtherapie führt zu langanhaltender Verbesserung bei Mukoviszidose
Berlin (7. Juli 2023) — Der Schleim in den Atemwegen ist weniger zäh, die Entzündung in der Lunge geht deutlich zurück: Diese positiven und langanhaltenden Effekte kann eine Dreifachtherapie bei Patient:innen mit Mukoviszidose erzielen. Das belegen Forschende der Charité – Universitätsmedizin Berlin und des Max Delbrück Center jetzt in der Fachzeitschrift European Respiratory Journal*. Die
WEITERLESEN »
Strahlentherapie ist oft ebenso effizient wie die OP: Neues vom DEGRO-Kongress
Strahlentherapie ist oft ebenso effizient wie die OP: Neues vom DEGRO-Kongress Kassel (20. Juni 2023) — Auf dem diesjährigen 29. Kongress der Deutschen Gesellschaft für Radioonkologie (DEGRO) wer-den aktuelle Arbeiten vorgestellt, die den Prozess einer zunehmenden Therapieeffizienz illustrieren. Bekannt ist, dass die Strahlentherapie bei bestimmten Indikationen ebenso effizient wie die Operation ist, ein Beispiel ist
WEITERLESEN »
Mit dem schnellwirksamen Depot-Antipsychotikum Risperidon ISM® (Okedi®) die Therapiekontinuität verbessern
Klinik-Workshop „EinBlick Schizophrenie“: Holzkirchen (7. Juni 2023) — Kontinuität in der Betreuungssituation und der medikamentösen Therapie trägt maßgeblich zum Behandlungserfolg bei Patient*innen mit Schizophrenie bei. Depot-Präparate werden dabei eingesetzt, um die Therapieadhärenz zu verbessern und die therapeutische Beziehung zu intensivieren.1 Seit April 2022 ist in Deutschland die innovative, schnellwirksame Depot-Formulierung Risperidon ISM® (Okedi®) auf dem
WEITERLESEN »
Wie das Dexom G7 abstrakte Zahlen mit Farben greifbar macht – eine Praxissicht
Biofeedback: bessere Stoffwechseleinstellung, größere Motivation? Mainz (3. Mai 2023) — Vor etwa einem halben Jahr wurde in Deutschland die neueste Generation von smarten Glukosesensoren eingeführt: das Dexcom G7. Seine Entwicklung orientierte sich an Bedürfnissen von Menschen mit Diabetes – einfache Bedienung, alltagstaugliche Anwendung, diskrete Handhabung – und folgte dabei zugleich wissenschaftlichen Standards, etwa in Bezug
WEITERLESEN »
Meilenstein in der Parkinson-Forschung: Neuer Alpha-Synuclein-Test entdeckt die Nervenerkrankung vor dem Ausbruch
Meilenstein in der Parkinson-Forschung: Neuer Alpha-Synuclein-Test entdeckt die Nervenerkrankung vor dem Ausbruch Berlin (20. April 2023) — Erstmals lässt sich das fehlgefaltete Protein Alpha-Synuclein im Gehirnwasser von Menschen mit Parkinson nachweisen, schon vor Ausbruch der motorischen Symptome. Der neue Test könnte eine frühe und genaue Diagnose und Behandlung der Erkrankung ermöglichen, bevor das Gehirn zu
WEITERLESEN »
Verhütung: Hormon- und Kupferspirale zeigen nur geringe Unterschiede
Verhütung: Hormon- und Kupferspirale zeigen nur geringe Unterschiede Köln (19. April 2023) — Im Auftrag des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) hat ein interdisziplinäres Team von Wissenschaftlerinnen und Wissenschaftlern unter Federführung der Share to Care GmbH in Köln die Vor- und Nachteile von Kupferspiralen und Hormonspiralen zur Verhütung ungewollter Schwangerschaften untersucht. Ihr
WEITERLESEN »
Positiver Effekt der grünen Mittelmeerdiät auf die Aorta
Positiver Effekt der grünen Mittelmeerdiät auf die Aorta Leipzig (19. April 2023) — Eine Ernährung mit vielen Pflanzenstoffen fördert die Elastizität der Blutgefäße und wirkt deren Alterung entgegen. Ein internationales Forschungsteam mit Beteiligung der Universität Leipzig hat erstmals eine starke positive Wirkung der grünen, mediterranen Diät auf die Beschaffenheit der Hauptschlagader nachgewiesen. „Ein gesunder Lebensstil
WEITERLESEN »
Krankenhaus-Report: Reform der Klinikstrukturen kann wichtigen Beitrag zur Lösung von Personalproblemen leisten
Berlin (19. April 2023) — Die im Zuge der anstehenden Krankenhausreform geplante Verlagerung von Krankenhausbehandlungen in den ambulanten Bereich und die qualitätsorientierte Konzentration von Klinikleistungen auf weniger Standorte können auch wichtige Beiträge zur Lösung der Personalprobleme in den deutschen Krankenhäusern leisten. Das zeigt der aktuelle Krankenhaus-Report des Wissenschaftlichen Instituts der AOK (WIdO) zum Thema „Personal“.
WEITERLESEN »
Zweites Positionspapier der DIVI-Sektion Metabolismus und Ernährung publiziert
Berlin (19. April 2023) — Auf das erste folgt jetzt das zweite Positionspapier der Sektion Metabolismus und Ernährung: „In diesem Positionspapier fokussieren wir uns vor allem auf das laborchemische Monitoring der Makro- und Mikronährstoffzufuhr und ergänzen damit unsere erste Empfehlung vom April vergangenen Jahres“, erklärt Sektionssprecher Prof. Gunnar Elke, stellv. Direktor der Klinik für Anästhesiologie
WEITERLESEN »
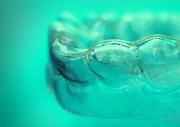
Intelligente Materialien für die Aligner-Therapie: nachhaltiger, kostengünstiger, schonender
Intelligente Materialien für die Aligner-Therapie: nachhaltiger, kostengünstiger, schonender Potsdam (19. April 2023) — Klinisch wirksam, maßgefertigt, unauffällig und komfortabel – die Anforderungen an Aligner für die Therapie von Zahnfehlstellungen sind hoch. So auch an das Material der Korrekturschienen. Ein Team des Fraunhofer-Instituts für Angewandte Polymerforschung IAP im Potsdam Science Park entwickelte nun zusammen mit dem
WEITERLESEN »
Die Rolle von Gebäuden bei der Ausbreitung von Infektionen
Braunschweig (17. April 2023) — Die weltweite Ausbreitung des Coronavirus hat deutlich gemacht: Zahlreiche Gebäude in Deutschland sind nicht auf Pandemien und die Eindämmung von Infektionsrisiken vorbereitet. Doch wo genau fehlen entsprechende Schutzmaßnahmen und wie können diese aussehen? Durch welche baulichen Eingriffe kann die Kontaktübertragung vermieden werden? Mit diesen Fragen beschäftigt sich das Projekt „SAVE“
WEITERLESEN »
Inhalations-Anästhetika machen Blut-Hirn- Schranke durchlässiger
München (13. April 2023) — In einem erfolgreich abgeschlossenen Förderprojekt der Wilhelm Sander-Stiftung untersuchten Forschende um Gesine Saher vom Max-Planck-Institut (MPI) für Multidisziplinäre Naturwissenschaften gemeinsam mit Kollegen aus Freiburg, Göttingen, Münster und Oldenburg, ob das Inhalations-Anästhestikum Isofluran einen speziellen Importweg über die Blut-Hirn-Schranke anschaltet. Dies unterstützt die Chemotherapie von Hirntumoren in Mäusen und könnte zur
WEITERLESEN »
Natriumaufnahme und Herz-Kreislaufrisiko
Kochsalzexzesse, aber auch starkes Salzsparen sind gesundheitlich riskant Berlin (12. April 2023) — Fast schon gebetsmühlenhaft raten Gesundheits- und Ernährungsorganisationen der allgemeinen Bevölkerung, ihren Kochsalzkonsum zu drosseln, um einem Bluthochdruck sowie Herz-Kreislauferkrankungen vorzubeugen. Solche Empfehlungen sind riskant, wie kanadische Forscher anhand einer umfassenden Datenanalyse dokumentieren. Denn zum einen gibt es keinen Beleg dafür, dass sich
WEITERLESEN »
Multiple Sklerose: Aktuelle Immunmodulatoren im Vergleich
Köln (12. April 2023) — Zur Behandlung von multipler Sklerose (MS) stehen einige Wirkstoffe mit Einfluss auf das Immunsystem, sogenannte Immunmodulatoren zur Verfügung, die Symptome und Folgen der entzündlichen und neurodegenerativen Erkrankung mindern und aufhalten sollen: Manche davon sind seit den 1990er-Jahren als Basistherapie im Einsatz, zum Beispiel Beta-Interferone oder Glatirameracetat. Seit 2005 werden weitere
WEITERLESEN »
Hydromorphon Aristo® long ist das führende Präferenzpräparat bei Tumorschmerz
Berlin (11. April 2023) – Der Einsatz von Opioiden spielt insbesondere bei tumorbedingten Schmerzen eine zentrale Rolle im Schmerzmanagement. Aufgrund pharmakologischer Vorteile in der Verträglichkeit ist Hydromorphon in dieser Indikation gemäß der kürzlich aktualisierten Praxisleitlinie Präferenzsubstanz der Deutschen Gesellschaft für Schmerztherapie (DGS).(1) Als Präparat zur langfristigen Analgesie und 24-Stunden-Retardierung ist Hydromorphon Aristo® long in der
WEITERLESEN »
Altenpflege: Student entwickelt KI für die Wundversorgung
Bielefeld (6. April 2023) — Künstliche Intelligenz soll künftig dabei helfen, chronische Wunden optimal zu versorgen. Vor allem in der Altenpflege kann das den Heilungsverlauf verbessern und das Personal entlasten. Eine entsprechende Software-Lösung entwickelt Julien Maarten Akay derzeit im Rahmen seines Forschungsmasterstudiums Data Science an der FH Bielefeld. Unterstützt wird Akay dabei von dem Paderborner
WEITERLESEN »
Erfolgreiche Erprobung empathischer Robotiksysteme in der Pflege
Offenburg (3. April 2023) — In dem vom Bundesministerium für Wirtschaft und Klimaschutz (BMWi) im Rahmen des Zentralen Innovationsprogramms für den Mittelstand (ZIM) geförderten Forschungsprojekt EmoCare wurde in den vergangenen zwei Jahren ein empathisches Robotiksystem für den Einsatz in Pflegeeinrichtungen entwickelt. Dieses innovative System kann anhand spezifischer Sensoren Emotionen und mentale Zustände wie Freude, Trauer,
WEITERLESEN »
Würzburger Neurowissenschaftler erhält Nachwuchspreis für Tremor-Studie
Würzburg (31. März 2023) — Wenn das Schreiben per Hand, Aufschließen der Haustür oder das Führen der Teetasse zum Mund zu einer Zitterpartie wird, kann die Ursache ein so genannter Essentieller Tremor sein. Ein Prozent der Bevölkerung ist von dem unkontrollierten Zittern betroffen, das sich meistens auf Arme und Hände, aber auch auf Beine und
WEITERLESEN »
Neue Leitlinie zur Diagnostik und Therapie von Asthma speziell für Fachärztinnen und -ärzte veröffentlicht
Berlin (31. März 2023) — Es gibt ab sofort eine verbesserte Entscheidungshilfe für eine gezielte, moderne Asthma-Therapie, die auch relevante Themen wie Berufswahl und digitale Unterstützungssysteme neu berücksichtigt: Die jetzt veröffentlichte und umfassend überarbeitete S2k-Leitlinie „Fachärztliche Diagnostik und Therapie von Asthma“ richtet sich in erster Linie an pneumologisch tätige Fachärztinnen und -ärzte und wird heute
WEITERLESEN »
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Düsseldorf/Berlin (29. März 2023) — Es geht um die Zukunft der Pneumologie: Heute ist der wichtigste Kongress für die Lungen- und Beatmungsmedizin mit 4.400 Teilnehmenden im Congress Center Düsseldorf gestartet. Bis Samstag werden in rund 100 Symposien sowie Poster-Präsentationen aktuelle Themen und die neuesten Erkenntnisse aus dem breitgefächerten Themengebiet der Pneumologie diskutiert. Rund 650 hochkarätige
WEITERLESEN »
WHO veröffentlicht erstmalig weltweit gültige Ausbildungsstandards für Anthroposophische Medizin
Berlin/Brüssel (29. März 2023) — Als Reaktion auf die weltweit steigende Nachfrage der Anthroposophischen Medizin hat die Weltgesundheitsorganisation (WHO) im März 2023 erstmalig global gültige Ausbildungsstandards (Benchmarks) für die Anthroposophische Medizin veröffentlicht. Die Benchmarks beschreiben Zugangskriterien zu den Ausbildungen, Ausbildungsinhalte und Ausbildungsdauer. Diese durch die WHO qualifizierten Standards machen die Relevanz der Anthroposophischen Medizin als
WEITERLESEN »
Verkehrslärm erhöht das Risiko für Suizid
Basel, Schweiz (29. März 2023) — Psychische Erkrankungen betreffen nahezu eine Milliarde Menschen weltweit und sind einer der Hauptgründe für Suizid. Eine Studie des Schweizerischen Tropen- und Public Health-Instituts (Swiss TPH) hat jetzt aufgezeigt, dass das Risiko für Suizid steigt, wenn Menschen hohem Verkehrslärm ausgesetzt sind. Die Ergebnisse wurden heute in der Fachzeitschrift Environmental Health
WEITERLESEN »
Geräusche von Inkubatoren auf der Intensivstation können das Gehör von Frühgeborenen schädigen
Kooperationsstudie der Universität Wien misst Pegel und Frequenzen von Geräuschen in Brutkästen Wien, Österreich (28. März 2023) — Eine Auswertung der üblichen Geräusche auf der Neugeborenen-Intensivstation ergab, dass die Inkubatoren zwar einige Geräusche dämpfen, aber auch einen dröhnenden Effekt bei niedrigen Frequenzen verursachen. Die Auswirkungen einer lauten Umgebung auf der Neugeborenen-Intensivstation sind zwar schon früher
WEITERLESEN »
Mit Blutzucker Strom erzeugen
Zürich, Schweiz (28. März 2023) — Wenn eine Brennstoffzelle unter der Haut Blutzucker aus dem Körper in elektrische Energie umwandelt, klingt das nach Science-Fiction. Dabei funktioniert es einwandfrei, wie ein ETH-Forschungsteam um den Biotechnologieprofessor Martin Fussenegger zeigt. Bei Typ-1-Diabetikern produziert der Körper kein Insulin. Deshalb müssen sich Betroffene das Hormon von aussen zuführen, um den
WEITERLESEN »
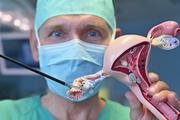
Mitralklappe reparieren: Chirurgisch oder mit Katheter?
Berlin (27. März 2023) –Eine undichte Mitralklappe kann grundsätzlich chirurgisch oder kathetergestützt repariert werden. Besonders häufig liegt ein sogenannter Mitralklappen-Prolaps vor, bei dem ein Teil der Klappe in den linken Vorhof vorfällt (prolabiert). Welche Methode zur Reparatur eines solchen Klappenschadens bei Patienten mit geringem Operationsrisiko am besten geeignet ist, untersucht die US-amerikanische PRIMARY-Studie. Den deutschen
WEITERLESEN »
Tierwohl-Fleisch aus Deutschland nur mäßig attraktiv in anderen Ländern
Forschungsergebnisse zeigen: Exportchancen von Tierwohl-Fleisch eher ernüchternd. Kriterien wie Herkunftsland, Qualität und Preis entscheidend. Braunschweig (27. März 2023) — Welche Ansprüche haben Verbraucherinnen und Verbraucher in anderen Weltregionen an Fleisch und welche Exportchancen hat Tierwohl-Fleisch aus Deutschland? Diese Fragen wurden am Thünen-Institut für Marktanalyse in Braunschweig in dem Forschungsprojekt „ExPoTiWo – Exportchancen von Tierwohl-Fleisch aus
WEITERLESEN »
Diät: Gehirn verstärkt Signal an Hungersynapsen
Mögliches Ziel für Medikamente zur Bekämpfung des Jo-Jo-Effekts Köln (24. März 2023) — Viele, die schon einmal eine Diät gemacht haben, kennen das: Nach der Diät kommt der Jojo-Effekt. Forschende vom Max-Planck-Institut für Stoffwechselforschung und der Harvard Medical School haben jetzt an Mäusen gezeigt, dass sich die Kommunikation im Gehirn während einer Diät ändert: Die
WEITERLESEN »
Neue Erkenntnisse für die Parkinson-Therapie
Mainz (22. März 2023) — Wissenschaftler der Sektion für Bewegungsstörungen und Neurostimulation der Klinik und Poliklinik für Neurologie der Universitätsmedizin Mainz haben eine wesentliche neue Erkenntnis zur Funktionsweise des Gehirns erzielt: Der sogenannte Nucleus subthalamicus, ein Nervenkern im Stammhirn, reguliert sowohl die Geschwindigkeit, mit der Bewegungen ausgeführt werden, als auch die Geschwindigkeit von Prozessen der
WEITERLESEN »
Süßigkeiten verändern unser Gehirn
Warum wir von Schokoriegeln und Co. nicht die Finger lassen können Köln (22. März 2023) — Schokoriegel, Chips und Pommes – warum können wir sie im Supermarkt nicht einfach links liegen lassen? Forschende des Max-Planck-Instituts für Stoffwechselforschung in Köln haben, in Zusammenarbeit mit der Yale University, jetzt nachgewiesen, dass Lebensmittel mit hohem Fett- und
WEITERLESEN »
Ethikrat: Gesundheitsdaten besser nutzen, ohne Datenschutz zu schwächen
Berlin (21. März 2023) — Am 22. März 2023 lädt der Deutsche Ethikrat zu einer öffentlichen Abendveranstaltung in der Reihe Forum Bioethik zum Thema „Patientenorientierte Datennutzung“. Ziel ist ein konstruktiver Dialog darüber, wie Gesundheitsdaten im Einklang mit dem Datenschutz für die medizinische Versorgung, die Personalisierung von Behandlungen und für die Forschung besser nutzbar gemacht werden
WEITERLESEN »
DGN warnt vor Botoxspritzen in die Magenwand zur Appetitzügelung und initiiert eine wissenschaftliche Aufarbeitung
Berlin (18. März 2023) — Nach einer Behandlung mit „Magen-Botox“ sind mehrere Menschen schwer an Botulismus, einer lebensbedrohlichen Botox-Vergiftung, erkrankt und werden in Deutschland neurointensivmedizinisch behandelt. Die DGN möchte Betroffene sowie Ärztinnen und Ärzte für die Symptome sensibilisieren, damit möglichst schnell eine Therapie eingeleitet werden kann. Fälle wie diese könnten zunehmen – Prof. Dr. Tim
WEITERLESEN »
Reform der Unabhängigen Patientenberatung und Änderung weiterer Gesetze
Berlin (16. März 2023) — Der Bundestag hat heute die Reform der Unabhängigen Patientenberatung Deutschland (UPD) beschlossen. Damit wird der Grundstein für die Neustrukturierung der UPD als Stiftung bürgerlichen Rechts gelegt. „Die Unabhängige Patientenberatung leistet mit ihrem Informations- und Beratungsangebot einen wichtigen Beitrag, um sich im Gesundheitssystem zurechtzufinden. Unabhängige Informationen sind essentiell, damit Patientinnen und
WEITERLESEN »
Bessere Versorgung von Schwangeren mit Vorstufe von Gebärmutterhalskrebs
Neuer Test ermöglicht Aussage über das Fortschreiten einer Krebsvorstufe Mannheim (15. März 2023) — Vorstufen von Gebärmutterhalskrebs treten vor allem bei Frauen zwischen 25 und 35 Jahren auf. Hauptrisikofaktor für die Entwicklung von Gebärmutterhalskrebs ist das Humane Papillomvirus (HPV). Ein operativer Eingriff ist die Behandlung erster Wahl. Bei schwangeren Frauen ist eine solche Operation jedoch
WEITERLESEN »
Zanubrutinib bei chronischer lymphatischer Leukämie: Zusatznutzen für bestimmte Betroffene
Köln (15. März 2023) — Zanubrutinib, ein Bruton-Tyrosinkinase-Inhibitor (BTK-Inhibitor) der zweiten Generation, ist für mehrere Anwendungsgebiete zugelassen. Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) hat nun untersucht, ob der Wirkstoff erwachsenen Patientinnen und Patienten mit chronischer lymphatischer Leukämie (CLL) nach einem Rezidiv oder bei einer refraktären, also nicht auf die bisherige Behandlung ansprechenden
WEITERLESEN »
Diabetes mellitus: eine der großen Volkskrankheiten im Blickpunkt der Schmerzmedizin
Deutscher Schmerz- und Palliativtag 2023 – ONLINE Berlin (15. März 2023) — Mit einer Prävalenz von etwa 10 % in der erwachsenen Bevölkerung in Deutschland zählt Diabetes mellitus zu den großen Volkskrankheiten.(1) Insbesondere bei schlechter Blutzuckerkontrolle leiden Betroffene im Krankheitsverlauf zunehmend unter Schmerzen – etwa aufgrund diabetischer Polyneuropathie, Durchblutungsstörungen oder Phantomschmerzen nach Fußamputation. Der hohen
WEITERLESEN »
Cochrane Review: Bewegung hilft, die Schwere von Bewegungssymptomen bei Parkinson zu lindern
Freiburg (15. März 2023) — „Hauptsache Bewegung!“ – So lässt sich ein aktueller Cochrane Review deutscher Autoren zusammenfassen, der die Wirksamkeit von Bewegungsangeboten für Menschen mit Morbus Parkinson untersucht. Die im Review ausgewertete Evidenz aus 156 randomisierten Studien spricht für günstige Auswirkungen solcher Angebote auf den Schweregrad von Bewegungssymptomen und die Lebensqualität. Die genaue Art
WEITERLESEN »
Sorgen und Versorgen – Schmerzmedizin konkret: „Sorge als identitätsstiftendes Element in der Schmerzmedizin“
Deutscher Schmerz- und Palliativtag 2023 – ONLINE Berlin (14. März 2023) — Unter dem Motto „Sorgen und Versorgen – Schmerzmedizin konkret“ begann heute mit dem Deutschen Schmerz- und Palliativtag 2023 das größte Kongressereignis zum Thema „Schmerz“ in Deutschland. Zum Auftakt gaben die Kongresspräsidenten Dr. Johannes Horlemann, Präsident der Deutschen Gesellschaft für Schmerzmedizin (DGS) e.V., und
WEITERLESEN »
Neue Erkenntnisse zur Differenzierbarkeit der Alzheimer Erkrankung – Warum Alzheimer nicht gleich Alzheimer ist
Heilbronn (14. März 2023) — Die Alzheimer Erkrankung wird vorrangig mit dem Verlust des Gedächtnisses in Verbindung gebracht. Doch leiden je nach Ausprägung und Schwere der Erkrankung auch eine Reihe weiterer geistiger Fähigkeiten mit unterschiedlich starken Auswirkungen für die Einzelnen. Hinzu kommt eine ganz individuelle Entwicklung des jeweiligen Krankheitsverlaufs. Wissenschaftler der Hochschule Heilbronn haben sich
WEITERLESEN »
Gesichtsverletzungen bei ukrainischen Flüchtlingen: Wie MKG-Chirurgen die Schluck-, Kau- und Sprechfunktion wiederherstellen
Parlamentarischer Abend der DGMKG: Experten berichteten über moderne Behandlungsmaßnahmen bei Schuss- und Explosionsverletzungen Berlin (14. März 2023) – Mehr als eine Millionen Flüchtlinge aus der Ukraine sind seit Kriegsbeginn bis Anfang März in Deutschland eingetroffen. Die Mehrheit darunter sind Frauen und Kinder – wenn Männer kommen, sind sie häufig durch Kriegseinsätze verletzt und müssen hierzulande
WEITERLESEN »
Intensivmedizin goes green – DGIIN rückt Nachhaltigkeit auf Intensivstationen in den Fokus
Köln/Berlin (14. März 2023) – Einwegartikel, umweltbelastende Substanzen und Geräte mit hohem Stromverbrauch – die Intensivmedizin ist einer der medizinischen Fachbereiche mit der problematischsten Umweltbilanz. Weil es gilt, kritisch kranken Menschen die medizinische Versorgung zukommen zu lassen, die sie brauchen, wurde der Ressourcenverbrauch bislang nur wenig hinterfragt. Doch das ändert sich derzeit: Sowohl international als
WEITERLESEN »
Post-COVID – die Deutsche Gesellschaft für Neurologie (DGN) rät derzeit von Apheresetherapien ab
Berlin (14. März 2023) – Studien gehen davon aus, dass bis zu 10 Prozent aller COVID-19-Erkrankten Post-COVID-Symptome davontragen könnten. Häufig handelt es sich um neurologische Beschwerden wie Konzentrationsstörungen, Fatigue oder Schmerzen. Weder ist die Ursache geklärt, noch gibt es kausale Therapieoptionen, deren Nachweis belegt ist. Auch Aphereseverfahren (Blutwäsche) können nach Ansicht der Deutschen Gesellschaft für
WEITERLESEN »
Technische Innovationen für eine maßgeschneiderte Parkinson-Diagnostik und Therapie
Berlin (14. März 2023) — Individualisierte Therapieentscheidungen gewinnen bei der Parkinson-Behandlung an Bedeutung. „Neue Technologien wie Sensoren und innovative Bildgebungsverfahren bieten vielversprechende Möglichkeiten, die Diagnose und die Behandlung von Betroffenen zu individualisieren und noch präziser zu gestalten“, sagte Prof. Alexander Storch, 2. Vorsitzender und Kongresspräsident der Deutschen Gesellschaft für Parkinson und Bewegungsstörungen (DPG) anlässlich des
WEITERLESEN »
Biomarker und Gene: neue Chancen und Herausforderungen für die Parkinson-Diagnose und spezifische Therapien
Berlin (14. März 2023) — Die Zukunft der Parkinson-Behandlung liegt in zielgerichteten Therapien, die an der Ursache ansetzen. Dabei wächst der Stellenwert von Genetik und Biomarkern in der Parkinson-Forschung. „Neue Biomarker zur Einordnung der vorherrschenden Pathologie und Stoffwechselwege sind zum Beispiel für klinische Studien im Bereich neuer Wirkstoffe sehr wichtig“, sagt PD Dr. Kathrin Brockmann,
WEITERLESEN »
Heilung in Sicht? Fortschritte auf dem Weg zur kausalen Therapie
Berlin (14. März 2023) — Ob Parkinson in Zukunft heilbar sein wird, ist eine zentrale Frage aktueller Forschung: „2022 wurden drei randomisierte, placebo-kontrollierte, doppelblinde, internationale multizentrische Phase-2-Studien veröffentlicht, die kausale Therapieansätze beim idiopathischen Parkinson-Syndrom (IPS) untersucht haben“, schilderte Prof. Uwe Walter, stellv. Direktor der Klinik und Poliklinik für Neurologie an der Universitätsmedizin Rostock auf dem
WEITERLESEN »
Unliebsame Arbeiten besser am Stück erledigen
Vallendar (14. März 2023) — Nicht alle Aufgaben, die täglich zu erledigen sind, machen Spaß – manche sind einfach nur anstrengend. Sollte daher an Tagen mit hoher Arbeitsbelastung lieber die ein oder andere angenehmere Aufgabe eingeschoben werden? Würde das die Motivation an Tagen mit hoher Arbeitsbelastung steigern? Eine wissenschaftliche Studie kommt zum gegenteiligen Ergebnis: Unangenehme
WEITERLESEN »
Eileiter-Entfernung als Vorbeugung gegen Eierstockkrebs akzeptiert
Jena (14. März 2023) — Frauen mit abgeschlossener Familienplanung können sich bei geplantem Unterleibseingriff die Eileiter vorbeugend entfernen lassen. Die hormonproduzierenden Eierstöcke bleiben dabei erhalten. Diese Maßnahme kann das Risiko für Eierstockkrebs wesentlich senken. Eine von der Frauenklinik des Universitätsklinikums Jena initiierte Untersuchung kommt zu dem Ergebnis, dass sich das Verfahren zu einem routinemäßigen Präventionsstandard
WEITERLESEN »
Intelligenter Roboter zur Handdesinfektion
Kiel (13. März 2023) — Forscher der Universität zu Lübeck, der Fachhochschule (FH) Kiel und der Süddänischen Universität Odense haben im Rahmen des Interreg-Projektes „Hand Disinfection Robot – HanDiRob“ einen intelligenten sozialen Roboter entwickelt, der Handdesinfektionsmittel anbietet und dessen Nutzung belohnt. Der Roboter könnte in Kliniken die Prävention gegen Infektionskrankheiten unterstützen. Die korrekte Desinfektion von
WEITERLESEN »
Antibiotika als Störfaktor bei CAR-T-Zell-Therapie
Regensburg (13. März 2023) — Die Gabe von CAR-T-Zellen gehört zu den vielversprechendsten Therapieoptionen bei Patienten mit bösartigen Erkrankungen des blutbildenden Systems. Zusammen mit einem internationalen Team von Wissenschaftlern ist es Professor Dr. Hendrik Poeck, Geschäftsführender Oberarzt der Klinik und Poliklinik für Innere Medizin III des Universitätsklinikums Regensburg (UKR), gelungen zu beweisen, dass die Gabe
WEITERLESEN »
Problem Schmerzmittelkonsum
Köln (10. März 2023) — In vielen Bereichen des Spitzen- und Leistungssports ist das Thema „Schmerzmittelkonsum“ zu einem Problem geworden – dies zeigt die weltweite Literaturrecherche einer Köln-Koblenzer Forschungsgruppe um Prof. Dr. Dr. Dieter Leyk, in der die Daten von über 6.000 Studien ausgewertet wurden. Die Ergebnisse wurden jetzt im Deutschen Ärzteblatt publiziert. Schätzungsweise 1,9
WEITERLESEN »
Cochrane Review: So lassen sich bei älteren Menschen Stürze verhindern
Freiburg (10. März 2023) — Die Beseitigung von Stolperfallen in der Wohnung kann das Sturzrisiko älterer Menschen um etwa ein Viertel verringern, so das Ergebnis eines aktuellen Cochrane Reviews. Für eine Reihe anderer Maßnahmen zur Verringerung des Sturzrisikos fand die Studie keine überzeugenden Belege. Stürze häufen sich im Alter: Schätzungen zufolge erleidet rund ein Drittel
WEITERLESEN »