MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Neue Formulierung von Bosentan zur kindgerechten PAH-Therapie
Weimar (4. Oktober 2009) – Die europäische Arzneimittelagentur EMEA (European Medicines Agency) hat der neuen, teilbaren und dispergierbaren 32 mg-Tablette von Bosentan (Tracleer®) die Zulassung erteilt. Diese neue Darreichungsform zur Herstellung einer Suspension wurde im Rahmen der FUTURE-1-Studie bei Kindern mit pulmonal arterieller Hypertonie ab zwei Jahren untersucht. Mit der Zulassung der 32 mg-Tablette durch die EMEA ist Bosentan das erste und einzige PAH-Therapeutikum mit geeigneter Formulierung für Kinder ab 2 Jahren. Zurzeit ist der orale duale Endothelin-Rezeptor-Antagonist Bosentan in Europa für die Behandlung der pulmonal arteriellen Hypertonie (PAH) der WHO-Funktionsklassen II und III zugelassen. Außerdem reduziert Bosentan die Anzahl neuer digitaler Ulzerationen bei Sklerodermie-Patienten, die an digitalen Ulzerationen leiden (Tracleer®-Fachinformation).
Pulmonal arterielle Hypertonie im Kindesalter ist eine schwerwiegende Erkrankung. Bleibt sie nach der Diagnosestellung unbehandelt, ist von einer geschätzten mittleren Überlebensdauer von 10 Monaten auszugehen (D’Alonzo 1991). Bislang gab es keine spezielle Darreichungsform eines PAH-Medikaments, die eine kindgerechte Dosierung gewährleisten konnte. Tracleer® ist nun die einzige PAH-Therapieoption, die in Deutschland in Form einer speziellen dispergierbaren und teilbaren Formulierung verordnet werden kann. Die Pharmakokinetik, Verträglichkeit und Sicherheit der neuen Formulierung wurden in der FUTURE-Studie (Pediatric FormUlation of bosenTan in pUlmonary arterial hypeRtEnsion) untersucht. Das Sicherheitsprofil entsprach dem bei erwachsenen Patienten mit PAH (Beghetti 2007).
FUTURE-1-Studie
Die FUTURE-1-Studie war eine offene, multizentrische, nicht-kontrollierte Studie der Phase III. An der Studie nahmen 36 Patienten (Alter: >= 2 und < 12 Jahre) teil, die an idiopathischer oder familiärer PAH erkrankt waren. Vier Wochen lang erhielten die Patienten 2 x täglich 2 mg/kg KG Bosentan in der neuen Darreichungsform (oral, dispergierbar, vierfach teilbar). Die Dosis wurde in den darauf folgenden vier Wochen auf 2 x täglich 4 mg/kg KG bis Woche 12 erhöht.
Als primärer Endpunkt wurde die AUCtau (area under the plasma-concentration-time-curve for a dosing intervall) von Bosentan in Woche 12 bestimmt. Sekundäre Endpunkte waren Parameter zur Verträglichkeit und weitere pharmakokinetische Parameter. Zu den explorativen Endpunkten zählten die Veränderung vom Ausgangswert bis Woche 12, was die vom Gesundheitszustand abhängige Lebensqualität, die WHO-Funktionsklasse und den allgemeinen klinischen Eindruck anbelangt.
Gut verträglich und wirksam
Die Studienergebnisse zeigen, dass die mit Bosentan erreichten Expositions-Levels in pädiatrischen und adulten Patienten unterschiedlich waren. Die erreichte Bosentan-Exposition war dosisunabhängig: Patienten, die 2 x täglich 2 mg/kg KG erhielten, kamen auf die gleichen Plasma-Spiegel wie diejenigen, die 2 x täglich 4 mg/kg KG erhielten. Die pädiatrische Bosentan-Formulierung wurde gut vertragen, das Sicherheits- und Verträglichkeitsprofil war mit dem in vorangegangenen plazebokontrollierten klinischen Studien bei erwachsenen Patienten vergleichbar.
Was die explorativen Endpunkte anbelangt, zeigte sich bei der Mehrheit der Patienten unter Bosentangabe ein verbessertes oder zumindest gleichbleibendes Befinden (erhoben mittels SF-10-Fragebogen „gesundheitsabhängige Lebensqualität“, WHO-Funktionsklassen-Analyse und Beurteilung des klinischen Gesamteindrucks durch Eltern und behandelnde Ärzte) (Berger 2008). Dabei ist mit Blick auf die Progressivität und maligne Natur der Erkrankung bei pädiatrischen Patienten bereits eine Stabilisierung des Zustands als Therapieerfolg zu werten.
Ergebnisse der Beurteilung durch Eltern und Ärzte
|
|
n |
eindeutig besser |
besser |
unverändert |
schlechter |
eindeutig schlechter |
|
Eltern |
35 |
7 |
11 |
13 |
1 |
2 |
|
Ärzte |
35 |
2 |
13 |
18 |
1 |
1 |
Prof. Dr. med. Dietmar Schranz, Kinderkardiologe, Gießen:
„Pädiatrische Patienten verstoffwechseln Medikamente anders als erwachsene Patienten. Diese Erkenntnis ist nicht neu, dennoch gibt es aktuell immer noch viel zu wenig speziell für Kinder entwickelte Darreichungsformen. Denn Studien mit Kindern sind vielen pharmazeutischen Unternehmen zu teuer, zu aufwändig und letztlich, da eine begrenzte Zielgruppe betreffend, nicht ausreichend effektiv. Daher begrüßen wir es, dass auf der Basis der FUTURE-1-Studie eine pädiatrische Formulierung von Bosentan entwickelt werden konnte. Damit können auch unsere kleinen Patienten von den Fortschritten in er PAH-Therapie profitieren, was bei einer Erkrankung mit dieser ernsten Prognose von großer Bedeutung ist.“
Dr. med. Martine Clozel, Kinderärztin und Chief Scientific Officer von Actelion, Allschwil:
„Unser Team ist sehr stolz auf diesen Erfolg. Schon in der frühen Entwicklungsphase von Tracleer haben wir beschlossen, uns mit der Entwicklung einer Formulierung für die tägliche Behandlung von Kindern, die unter PAH leiden, zu befassen – selbst wenn diese Patientenpopulation sehr klein ist. Es war ein langer, aber schlussendlich lohnender Weg, auf den wir uns noch vor der ersten Marktzulassung von Tracleer begeben hatten.“
–
PAH bei Kindern
Die seltene Erkrankung Lungenhochdruck kann nicht nur im Erwachsenenalter, sondern auch im Kindesalter auftreten. Bei Kindern kommen meist folgende Formen vor:
Pulmonal arterielle Hypertonie (PAH) assoziiert mit angeborenen Herzfehlern
Lungenhochdruck kann sich auch nach der erfolgreichen Operation eines angeborenen Herzfehlers entwickeln. Betroffene Kinder oder Erwachsene, die eine Operation aufgrund eines Herzvitiums hinter sich haben, sollten regelmäßig untersucht werden, um einen eventuellen Lungenhochdruck frühzeitig festzustellen und behandeln zu können. Bei Shuntvitien wird die Lunge vermehrt durchblutet, so dass durch die Volumenbelastung in den Lungengefäßen der Druck steigt, es entsteht ein pulmonal arterieller Hochdruck. Im Verlauf der Erkrankung kann es zur Shunt-Umkehr (Eisenmenger-Reaktion) kommen.
Idiopathische oder hereditäre PAH
Bei der idiopathischen PAH ist die Ursache nicht bekannt.
Bei der hereditären PAH sind Genveränderungen die möglich Ursache für die familiäre Häufung dieser Erkrankung. Ist ein Elternteil an einer erblichen Form erkrankt, beträgt die Erkrankungswahrscheinlichkeit für das Kind fünf bis zehn Prozent.
Im Kindesalter gilt für beide Formen, dass sie häufig erst im Spätstadium erkannt werden, weil die erkrankten Kinder lange Zeit beschwerdefrei sind oder ihre Beschwerden oft fälschlicherweise einem Asthma zugeordnet werden. Bei den betroffenen Kindern finden sich nur selten auffällige Herzgeräusche, daher ist es für Pädiater relativ schwierig, die Erkrankung frühzeitig zu erkennen.
Persistierende pulmonale Hypertonie des Neugeborenen (PPHN)
Kommt es postnatal zu einer inkompletten Trennung des Körper- und Lungenkreislaufes, entsteht eine pulmonal arterielle Hypertonie. Wird diese rasch behandelt, kommt es in der Regel zur vollständigen Genesung.
Abbildungen

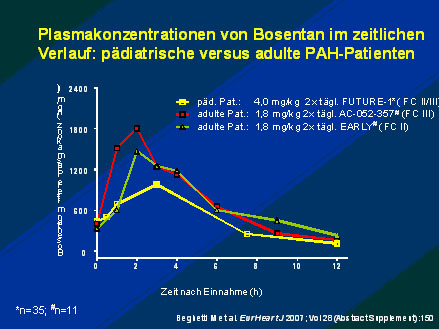
Abb. 1: Plasmakonzentrationen von Bosentan im zeitlichen Verlauf: pädiatrische versus adulte PAH-Patienten.

Abb. 2: Absorptionsplateau von Bosentan: 2 und 4 mg/kg 2 x täglich (pädiatrische Patienten).
Literaturhinweise
-
Barst RJ et al.: Clin Pharmacol Ther 2003;73:372-82
-
Beghetti M et al.: FUTURE-1 study. Eur Heart J 2007;28 (Abstract Supplement):150
-
Berger RMF et al.: Cardiol Young 2008; 18 (Abstract 08-8, AEPC Kongress 2008 in Venedig)
-
D’Alonzo G et al.: Ann Intern Med 1991;115:343-349.
-
Tracleer®-Fachinformation
Webcast mit internationalen Experten für mehr Informationen
Unter http://packerforbes.intra.tv/actelion können Sie sich einen webcast (in englischer Sprache, Dauer: ca. 20 Min.) ansehen, der über folgende Themen informiert:
-
The role of the industry in developing pediatric medicines , Prof. William van’t Hoff, Great Britain
-
A case in point: Pediatric PAH, Prof. Damien Bonnet, France
-
A case in point: Tracleer in PAH, Prof. Maurice Beghetti, Switzerland
Quelle: Actelion-Symposium zum Thema „Therapie von Anfang an – pulmonal arterielle Hypertonie (PAH) bei Kindern und Jugendlichen“ am 04.10.2009 in Weimar, anlässlich des Kongresses der Deutschen Gesellschaft für pädiatrische Kardiologie (DGPK) (Cramer-Gesundheits-Consulting) (tB).