MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Pembrolizumab bei Lungenkrebs: Hinweis auf beträchtlichen Zusatznutzen
Gegenüber Docetaxel überwiegen Vorteile deutlich Gegenüber Best supportive Care Zusatznutzen nicht belegt Köln (16. November 2016) – Pembrolizumab (Handelsname Keytruda) wurde zunächst für die Behandlung von schwarzem Hautkrebs eingeführt. Seit Juli 2016 steht der monoklonale Antikörper auch für Erwachsene mit lokal fortgeschrittenem oder metastasierendem nicht kleinzelligem Lungenkarzinom (NSCLC) zur Verfügung, deren Tumoren den T-Zell-Rezeptor-Liganden PD-L1
WEITERLESEN »
Roche Pharma: FDA-Zulassung für Atezolizumab bei fortgeschrittenem NSCLC
Grenzach-Wyhlen (21 . Oktober 2016) – Die US-Zulassungsbehörde FDA hat Atezolizumab als ersten Anti-PD-L1-Antikörper überhaupt zur Behandlung von Patienten mit metastasiertem nicht-kleinzelligem Bronchialkarzinom (NSCLC) zugelassen. Bereits vorbehandelten NSCLC-Patienten bietet Atezolizumab einen signifikanten Überlebensvorteil gegenüber Docetaxel – das belegt unter anderem eine Interimsanalyse der Phase-III-Studie OAK, die kürzlich auf dem ESMO vorgestellt wurde.1 Bereits im Mai
WEITERLESEN »
XALKORI® (Crizotinib) erhält Zulassung für die Therapie des fortgeschrittenen ROS1-positiven nichtkleinzelligen Lungenkarzinoms (NSCLC) in der Europäischen Union (EU)
Crizotinib ist die erste und einzige zugelassene zielgerichtete Therapie zur Behandlung von Patienten mit fortgeschrittenem ROS1-positiven NSCLC in der EU New York / Berlin (5. September 2016) – Die Europäische Kommission hat die Zulassung für Crizotinib (Handelsname Xalkori®) erweitert: Das Medikament ist damit in der Europäischen Union (EU) nun auch zur Behandlung von erwachsenen Patienten
WEITERLESEN »
Vorteile beim Gesamtüberleben und bei den Nebenwirkungen: Nivolumab bei fortgeschrittenem Lungenkarzinom: Hinweis auf erheblichen Zusatznutzen
Köln (1. August 2016) – Nivolumab ist seit April 2016 als sogenannter Checkpoint-Inhibitor zur Behandlung Erwachsener mit lokal fortgeschrittenem oder metastasiertem nichtkleinzelligem Lungenkarzinom (NSCLC) mit nicht plattenepithelialer Histologie zugelassen, die bereits eine Chemotherapie durchlaufen haben. In einer frühen Nutzenbewertung hat das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) nun untersucht, ob der monoklonale Antikörper
WEITERLESEN »
Afatinib bei fortgeschrittenem Plattenepithelkarzinom der Lunge: Zusatznutzen nicht belegt
Vorgelegte Vergleiche für die Nutzenbewertung ungeeignet Köln (1. August 2016) – Afatinib (Handelsname Giotrif) ist seit April 2016 zur Behandlung Erwachsener mit lokal fortgeschrittenem oder metastasiertem nichtkleinzelligem Lungenkarzinom (NSCLC) mit Plattenepithel-Histologie zugelassen, die bereits eine Chemotherapie durchlaufen haben. In einer frühen Nutzenbewertung hat das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) nun untersucht, ob
WEITERLESEN »
Zulassungserweiterung für Avastin zur Behandlung von EGFR-positivem NSCLC Avastin plus Tarceva verlängert signifikant das PFS
Berlin (21. Juli 2016) – Die Europäische Kommission hat am 2. Juni 2016 die Zulassungserweiterung für Avastin® (Bevacizumab) in Kombination mit Tarceva® (Erlotinib) erteilt. Die Kombination ist zugelassen zur First-Line-Therapie von inoperablem, fortgeschrittenem, metastasiertem oder rezidivierendem EGFRMutations-positivem nicht-kleinzelligem, Nicht-Plattenepithel-Lungenkarzinom (nsNSCLC).1 In der zulassungsrelevanten Studie JO25567 konnte eine signifikante Verlängerung des progressionsfreien Überlebens (PFS) auf 16,0
WEITERLESEN »
Necitumumab bei NSCLC: Hinweis auf geringen Zusatznutzen für Patienten mit Metastasen
Nachteile bei Nebenwirkungen heben Vorteil beim Gesamtüberleben nicht auf Köln (1. Juli 2016) – Der monoklonale Antikörper Necitumumab ist seit Februar 2016 zugelassen zur Behandlung von Patienten mit lokal fortgeschrittenem oder metastasiertem, den epidermalen Wachstumsfaktor-Rezeptor (EGFR) exprimierendem, nicht kleinzelligem Lungenkrebs (NSCLC), die bislang keine Chemotherapie für dieses Stadium ihrer Erkrankung erhalten haben. Der Wirkstoff wird
WEITERLESEN »
Erste Ergebnisse der J-ALEX-Studie auf ASCO 2016 präsentiert: Alectinib wirksam bei ALK-positivem NSCLC
Hamburg (22. Juni 2016) – Alectinib führt im Vergleich zu Crizotinib zu einer signifikanten Verlängerung des progressionsfreien Überlebens (PFS) bei Patienten mit ALK*-positivem fortgeschrittenem NSCLC+.1 Dies zeigen erste Daten der J-ALEX-Studie, die auf der diesjährigen ASCO (American Society of Clinical Oncology)-Jahrestagung vorgestellt wurden. Die Studie untersuchte die Wirksamkeit und Verträglichkeit von Alectinib in der First-Line-Therapie.
Keine direkt vergleichenden Studien: Osimertinib bei Lungenkrebs: Zusatznutzen nicht belegt
Effekte in historischen Vergleichen zu klein für Aussagen zum Zusatznutzen Köln (15. Juni 2016) – Osimertinib ist seit Februar 2016 zur Behandlung erwachsener Patienten mit lokal fortgeschrittenem oder metastasiertem, nicht kleinzelligem Lungenkarzinom (NSCLC) und einer T790M-Mutation des epidermalen Wachstumsfaktor-Rezeptors (Epidermal Growth Factor Receptor, EGFR) zugelassen. In einer frühen Nutzenbewertung hat das Institut für Qualität und
WEITERLESEN »
Verbesserte Versorgung von Lungenkrebspatienten durch Liquid Biopsy – Lungennetzwerk NOWEL schließt Vertrag mit der BARMER GEK
Oldenburg (20. Mai 2016) – Das Lungennetzwerk NOWEL, ein Zusammenschluss führender Experten aus den Bereichen Onkologie, Pneumologie und Pathologie, hat mit der BARMER GEK einen Vertrag zur besonderen Versorgung abgeschlossen, um Patienten deutschlandweit Zugang zu einer umfassenden molekularen Tumordiagnostik an Blut („Liquid Biopsy“) zu gewährleisten. Das genetische Profil des individuellen Tumors, das die Grundlage der
WEITERLESEN »
Bronchialkarzinom: Zusatznutzen von Crizotinib zur Erstbehandlung nicht belegt
Kontrollarm der einzigen Studie bildet zweckmäßige Vergleichstherapie nicht adäquat ab Köln (1. April 2016) – Seit 2012 steht der Wirkstoff Crizotinib (Handelsname Xalkori) Patientinnen und Patienten mit fortgeschrittenem nicht kleinzelligem Lungenkrebs (Bronchialkarzinom) zur Verfügung, die eine hohe Aktivität des Enzyms anaplastische Lymphomkinase (ALK) aufweisen und bereits mit einer anderen Therapie vorbehandelt sind. Im November 2015
WEITERLESEN »
Rote-Hand-Brief zu Tarceva® (Erlotinib): Einschränkung des Anwendungsgebiets
Bonn (14. Januar 2016) – Das Anwendungsgebiet von Tarceva® wurde in der Erhaltungstherapie des lokal fortgeschrittenen oder metastasierten nicht-kleinzelligen Lungenkarzinoms (NSCLC) beschränkt auf Patienten mit Tumoren, die eine aktivierende EGFR-(epidermaler Wachstumsfaktorrezeptor)-Mutation aufweisen. Die vom CHMP verabschiedeten Vorgaben sind auf nationaler Ebene übernommen worden. Die Roche Pharma AG informiert in einem Rote-Hand-Brief über diese wichtige Änderung.
Nivolumab bei Lungenkarzinom: Hinweis auf erheblichen Zusatznutzen für unter 75-Jährige
Unter 75-Jährige mit gutem Allgemeinzustand überleben deutlich länger Bei Älteren Anhaltspunkt für nicht quantifizierbaren Zusatznutzen Köln (16. November 2015) – Nivolumab ist ein antitumoraler Wirkstoff aus der Gruppe der monoklonalen Antikörper. Er ist seit Juni 2015 unter dem Handelsnamen Opdivo für Erwachsene mit fortgeschrittenem schwarzem Hautkrebs und seit Juli 2015 unter dem Handelsnamen Nivolumab BMS
WEITERLESEN »
Positive Ergebnisse einer aktuellen Analyse der Studien LUX-Lung 3 & 6: CHMP empfiehlt Update der Zulassung von Giotrif®
CHMP empfiehlt die Aktualisierung der europäischen Zulassung auf Basis einer aktuellen Analyse der LUX-Lung 3- und 6-Studien. Die Daten der aktuellen Analyse stärken die derzeit vorliegenden Ergebnisse zu PFS (progressionsfreies Überleben = primärer Endpunkt), Symptomkontrolle und OS (Gesamtüberleben = sekundärer Endpunkt). Für Patienten mit der häufigsten EGFRA-Mutation (Del19) lag der Überlebensvorteil in der Erstlinientherapie
WEITERLESEN »
ALK-Inhibitor und Immuntherapie zeigen vielversprechende Ergebnisse
Bonn (16. Juni 2015) – Aktuelle, auf der 51. Jahrestagung der American Society of Clinical Oncology (ASCO) vom 29. Mai bis 2. Juni 2015 in Chicago/Illinois, USA, vorgestellte Daten sprechen dafür, dass in der Behandlung von Lungenkrebs zukünftig neue Wirkstoffe zur Verfügung stehen könnten. Den Studiendaten zufolge zeichnen sich die beiden neuen Prüfmedikamente Alectinib
WEITERLESEN »
Nintedanib bei Lungenkrebs: Zusatznutzen abhängig vom Schweregrad der Erkrankung
Vorteil für Patienten ohne Hirnmetastasen / Nachteile für Patienten mit Hirnmetastasen Köln (1. April 2015) – Seit November 2014 ist Nintedanib (Handelsname Vargatef) in Kombination mit Docetaxel zugelassen zur Behandlung von Erwachsenen mit fortgeschrittenem nicht-kleinzelligem Lungenkarzinom (NSCLC) im Drüsengewebe (Adenokarzinom), die bereits eine Chemotherapie erhalten haben. Das Institut für Qualität und Wirtschaftlichkeit im
WEITERLESEN »
Afatinib* (GIOTRIF ® ) bei bestimmten Formen des fortgeschrittenen NSCLC mit EGFR-Mutation – Daten und Erfahrungen
Afatinib* (GIOTRIF® ) bei bestimmten Formen des fortgeschrittenen NSCLC mit EGFR-Mutation Ingelheim (4. Februar 2015) – Mit der Zulassung von GIOTRIF® (Afatinib*) erfolgte ein wichtiger Schritt in der Erstlinientherapie von bestimmten Formen des fortgeschrittenen nicht-kleinzelligen Lungenkarzinoms (NSCLC) mit EGFRA -Mutation. Auf Grundlage der Daten von zwei randomisierten Phase-III-Studien wird der irreversible ErbB-Family-Blocker inzwischen seit rund
WEITERLESEN »
Nintedanib* (Vargatef™) erhält EU-Zulassung für NSCLC-Patienten mit fortgeschrittenem Adenokarzinom nach Erstlinien-Chemotherapie
Ingelheim (27. November 2014) – Die Europäische Kommission hat die Zulassung von Nintedanib* (Vargatef™) in Kombination mit Docetaxel zur Behandlung erwachsener Patienten mit lokal fortgeschrittenem, metastasiertem oder lokal rezidiviertem nicht-kleinzelligen Lungenkarzinom (NSCLC) mit Adenokarzinom-Histologie nach Erstlinien-Chemotherapie bekannt gegeben.
Fortgeschrittenes NSCLC: In allen Therapielinien umfassende Erfahrungen mit Erlotinib
Bremen (28. März 2014) – Beim lokal fortgeschrittenen oder metastasierten NSCLC ist Erlotinib (Tarceva®) als einziger EGFR-Tyrosinkinase-Inhibitor (TKI) für alle Therapielinien zugelassen. Die breite Zulassung ist ein Grund dafür, dass inzwischen weltweit mehr als eine Million Patienten mit Erlotinib behandelt wurden [1]. Der EGFR-TKI stellt heute sowohl bei chemotherapeutisch vorbehandelten als auch bei Chemotherapie-naiven Patienten mit
WEITERLESEN »
Lungenkrebspatienten mit Mutation Del19 profitieren am stärksten: Afatinib: Zusatznutzen vom Mutationsstatus abhängig
Köln (17. Februar 2014) – Seit September 2013 ist Afatinib (Handelsname GIOTRIF) zugelassen zur Behandlung von erwachsenen Patienten mit lokal fortgeschrittenem bzw. metastasiertem nicht-kleinzelligem Lungenkarzinom (NSCLC) mit aktivierenden EGF-Rezeptor-Mutationen, die noch nicht mit einem EGF-Rezeptor-Tyrosinkinase-Inhibitor (EGFR-TKI) behandelt wurden. Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) hat mit einer frühen Nutzenbewertung gemäß Arzneimittelmarktneuordnungsgesetz
WEITERLESEN »
Bessere Therapiemöglichkeiten bei Lungenkrebs
Köln/Bonn (27. Januar 2014) – Einem internationalen Forscherverbund ist es gelungen, die Überlebenschancen von Lungenkrebspatienten beträchtlich zu erhöhen – bei manchen Lungenkrebsarten sogar um das Dreifache. Möglich wurde dies durch moderne molekulargenetische Diagnoseverfahren, mit denen die Wissenschaftler Tumoren besser klassifizieren und die Therapie entsprechend anpassen konnten. Teil des Forscherteams aus 10 verschiedenen Ländern waren
WEITERLESEN »
BEYOND & AVAILABLE: Phase-III-Studie und NIS bestätigen Nutzen von Bevacizumab in der First-Line-Therapie des fortgeschrittenen nsNSCLC
Grenzach-Wyhlen (12. November 2013) – Die Kombination von Bevacizumab (Avastin) mit Carboplatin/Paclitaxel verringert im Vergleich zur alleinigen Chemotherapie das Progressionsrisiko um 60 %; parallel hierzu wird das mediane progressionsfreie Überleben auf 9,2 Monate verlängert. Dies zeigen die Ergebnisse der Phase-III-Studie BEYOND, die ebenso wie die erste Interimsanalyse der nicht-interventionellen Studie (NIS) AVAILABLE kürzlich bei der
WEITERLESEN »
Qiagen: RGQ PCR-Kit als Begleitdiagnostikum für Lungenkrebspatienten
Hilden, Deutschland / Germantown, Maryland, USA (12. Juli 2013) – QIAGEN N.V. (NASDAQ: QGEN; Frankfurt Prime Standard: QIA) hat heute bekannt gegeben, dass das Unternehmen von der US-amerikanischen Food and Drug Administration (FDA) die Zulassung zur Vermarktung des therascreen® EGFR-Tests als Begleitdiagnostikum zur Steuerung von GILOTRIFTM (afatinib) erhalten hat, einer neuen gezielten Therapie von Boehringer
WEITERLESEN »
Ergebnisse von zwei großen Phase-III-Studien beim fortgeschrittenen nicht-kleinzelligen Lungenkarzinom (NSCLC) Post-ASCO vorgestellt
Erstlinientherapie: Afatinib* bestätigt in weiterer Phase-III-Studie eine Verbesserung des progressionsfreien Überlebens bei NSCLC-Patienten mit EGFR-Mutation Zweitlinientherapie: Nach fast 10 Jahren Überlebensvorteil für Patienten mit NSCLC gezeigt – Nintedanib* in Kombination mit Docetaxel in Phase III wirksam Frankfurt am Main (19. Juni 2013) – Auf dem diesjährigen Kongress der American Society of Clinical Oncology (ASCO) in
WEITERLESEN »
Bevacizumab-haltige Therapie beim fortgeschrittenen NSCLC als First-Line-Standard bestätigt und in neuen ESMO-Guidelines mit IA-Empfehlung bewertet
Hannover (22. März 2013) – First-Line-Schemata mit Bevacizumab (Avastin®) gelten heute beim fortgeschrittenen Nicht-Plattenepithel-NSCLC als Therapiestandard. Dieser hohe Stellenwert basiert unter anderem auf den Ergebnissen der Phase-III-Studien E4599 und PointBreak sowie den neuen ESMO-Guidelines. Die Bedeutung der aktuellen Studiendaten für die klinische Praxis und die Grundlagen der neuen ESMO-Empfehlungen erläuterten Dr. Claus-Peter Schneider, Bad
WEITERLESEN »
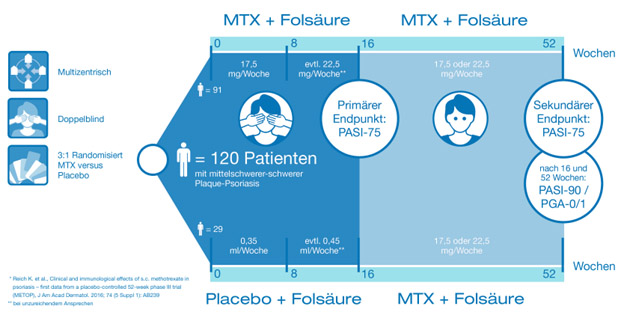
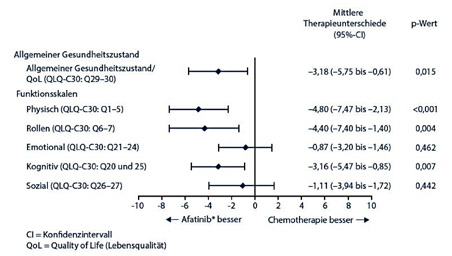
DGP-Kongress 2013: ErbB-Family-Blocker Afatinib* zeigt in Phase-III-Studie signifikante Vorteile bei Wirksamkeit und Symptomverbesserung gegenüber Vergleichschemotherapie: NSCLC entscheidend für Lebensqualität in der progressionsfreien Zeit
Hannover (21. März 2013) – Husten, Schmerzen und Atemnot – diese Symptome prägen das Krankheitsbild von Patienten mit nichtkleinzelligem Lungenkarzinom (NSCLC) und erhöhen ihren Leidensdruck zusätzlich. Wirksame Therapien für diese Patienten werden dringend benötigt. Die LUX-Lung 3-Daten zeigen eine effektive Verzögerung des Tumorwachstums in der Erstlinientherapie bei Patienten mit NSCLC und positivem EGFR-Mutationsstatus gegenüber
WEITERLESEN »
Zusatznutzen von Crizotinib ist nicht belegt
Köln (15. Februar 2013) – Der Wirkstoff Crizotinib (Handelsname Xalkori®) steht seit Oktober 2012 Patientinnen und Patienten mit fortgeschrittenem nicht kleinzelligem Lungenkrebs (Bronchialkarzinom) zur Verfügung, die eine hohe Aktivität der anaplastischen Lymphomkinase (ALK) aufweisen und bereits mit einer anderen Therapie vorbehandelt sind. Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) hat jetzt den
WEITERLESEN »
Nicht-kleinzelliges Lungenkarzinom (NSCLC): Laut Zulassungsstudie verzögert Afatinib* nicht nur die Tumorprogression, sondern steigert auch Lebensqualität und bessert tumorassoziierte Symptome
Wien, Österreich (29. September 2012) – Eine aktuelle Auswertung der Lux-Lung 3 Studie unterstreicht, dass Patienten mit einem fortgeschrittenem nicht-kleinzelligen Lungenkarzinom (NSCLC) und Mutationen im Epidermal Growth Factor Receptor (EGFR) von einer Erstlinienbehandlung mit Afatinib* profitieren können. Die auf dem Kongress der European Society for Medical Oncology (ESMO) 2012 in Wien präsentierten Daten zeigen,
WEITERLESEN »
Merck zieht EU-Zulassungsantrag für Erbitux bei NSCLC zurück
Darmstadt (18. September 2012) – Merck hat heute die strategische Entscheidung zur Rücknahme des Antrags bei der Europäischen Arzneimittelagentur (EMA) auf Indikationserweiterung für die Zulassung von Erbitux® in Kombination mit einer platinbasierten Standardchemotherapie in der Erstlinienbehandlung von Patienten mit fortgeschrittenem oder metastasiertem nicht-kleinzelligem Bronchialkarzinom (NSCLC) mit einer hohen Expression des epidermalen Wachstumsfaktorrezeptors (EGFR) bekannt
WEITERLESEN »
Afatinib zeigt in einer Zulassungsstudie bislang nicht erreichtes progressionsfreies Überleben in der Erstlinientherapie von Lungenkrebspatienten mit positivem EGFR-Mutationsstatus
Ergebnisse der Studie LUX-Lung 3 im Fokus der offiziellen ASCO-Pressekonferenz: Afatinib* verzögert die Tumorprogression signifikant länger als der beste Chemotherapie-Standard Ingelheim (4. Juni 2012) – Die Phase-III-Studie LUX-Lung 3 ergab, dass Patienten mit Lungenkarzinom, die den neuartigen irreversiblen ErbB-Family-Blocker Afatinib* als Erstlinientherapie erhielten, fast ein Jahr ohne Fortschreiten der Erkrankung blieben (mediane progressionsfreie
WEITERLESEN »
First-Line-Therapie des fortgeschrittenen NSCLC: Hohe Wirksamkeit von Bevacizumab bestätigt
Nürnberg (30. März 2012) – Die Wirksamkeit von Bevacizumab (Avastin®) in der First-Line-Therapie des nicht-kleinzelligen Lungenkarzinoms (NSCLC) wird mittlerweile durch zahlreiche Studienergebnisse bestätigt. In der aktuell vorgestellten INNOVATIONS-Studie zeigte sich, dass mit einem medianen Gesamtüberleben (OS) von 18 Monaten insbesondere die Subgruppe der Patienten ohne EGFR-Mutation von einer Bevacizumab-basierten Therapie profitieren. Lange Überlebenszeiten wurden
WEITERLESEN »
First-Line-Therapie des fortgeschrittenen NSCLC: Bevacizumab plus Cisplatin/Gemcitabin auch in der INNOVATIONS-Studie hoch wirksam
Grenzach-Wyhlen (9. Januar 2012) – Patienten mit fortgeschrittenem NSCLC, die für eine platinhaltige Chemotherapie in Frage kommen, profitieren vom zusätzlichen Einsatz des VEGF-Antikörpers Bevacizumab (Avastin®). Dies bestätigen die Ergebnisse der INNOVATIONS-Studie: Mit der Kombination Bevacizumab + Cisplatin/Gemcitabin erreichten Patienten ohne nachgewiesene EGFR-Mutation ein medianes Gesamtüberleben von 18 Monaten [1]. Damit belegt nun – nach der
WEITERLESEN »
First time Erlotinib first-line: Erlotinib jetzt zugelassen bei Patienten mit EGFR-Mutation
Hamburg (30. August 2011) – Am 1. September hat Erlotinib (Tarceva®) die europaweite Zulassung zur Erstlinientherapie beim fortgeschrittenen nicht-kleinzelligen Lungenkrebs (NSCLC) erhalten. Die Zulassungserweiterung ist relevant für Patienten mit aktivierenden Mutationen im epidermalen Wachstumsfaktorrezeptor (EGFR). Die Ergebnisse der zulassungsrelevanten EURTAC-Studie (European Tarceva Versus Chemotherapy Phase III Study) zeigten, dass diese Patienten first-line signifikant stärker
WEITERLESEN »
QIAGEN und Pfizer entwickeln Begleitdiagnostikum für ein neues Lungenkrebs-Präparat
Verbindung von Test und Medikament soll Behandlungsstandard für Patienten mit nicht-kleinzelligem Lungenkarzinom (NSCLC) verbessern Hilden (16. August 2011) – QIAGEN hat heute den Abschluss einer Kooperationsvereinbarung mit Pfizer Inc. bekanntgegeben. Gegenstand der Vereinbarung ist die Entwicklung eines molekularen therapiebegleitenden Tests für ein Präparat von Pfizer, das derzeit in weltweiten klinischen Studien zur Behandlung
WEITERLESEN »
Positives CHMP-Votum für Erlotinib in der Erstlinientherapie bei Patienten mit EGFR-Mutation
Grenzach-Wyhlen (25. Juli 2011) – Das CHMP (Comittee for Medicinal Products for Human Use) der europäischen Arzneimittelzulassungsbehörde EMA (European Medicines Agency) hat sich am 22. Juli 2011 für die erweiterte Zulassung von Erlotinib (Tarceva®) zur Erstlinientherapie beim fortgeschrittenen nicht-kleinzelligen Lungenkrebs (NSCLC) ausgesprochen. Die Empfehlung gilt für Patienten mit aktivierenden Mutationen des epidermalen Wachstumsfaktorrezeptors (EGFR).
WEITERLESEN »
Fortgeschrittenes NSCLC: First-Line-Therapie mit Erlotinib zeigt überlegene Wirksamkeit bei EGFR-positiven Patienten
Köln (17. Juni 2011) – Erlotinib (Tarceva®) verlängert signifikant das mediane progressionsfreie Überleben (PFS) von Patienten mit fortgeschrittenem NSCLC und einer EGFR-Mutation in der First-Line-Therapie gegenüber einer Platin-basierten Chemotherapie. Das zeigen die Ergebnisse der EURTAC-Studie (European Tarceva Versus Chemotherapy Phase III Study), die ihren primären Endpunkt bereits in der Interimsanalyse erreichte.
Ergebnisse sprechen für zielgerichtete Therapien: Bevacizumab und Erlotinib beim fortgeschrittenen NSCLC
Dresden (7. April 2011) – Die bis dato akkumulierten Daten zu Bevacizumab (Avastin®) und Erlotinib (Tarceva®) bestätigen den hohen Stellenwert der beiden zielgerichteten Therapien beim nicht-kleinzelligen Lungenkarzinom (NSCLC). So führt die Kombination einer platinhaltigen Chemotherapie mit Bevacizumab in der First-Line-Therapie zum bisher längsten medianen Gesamtüberleben von mehr als 14 Monaten bei Patienten mit Adenokarzinom.
WEITERLESEN »
Lungenkrebs frühzeitig erkennen
Leipzig (1. Februar 2011) – Je früher Krebserkrankungen erkannt werden, desto besser sind die Heilungschancen. Forscher entwickeln jetzt eine neue Diagnostikplattform, mit der sich die Krankheit auch beim Hausarzt schon im Frühstadium feststellen lassen soll: Proteinbiomarker in der Atemluft verraten die Gegenwart entarteter Zellen in der Lunge.
Erlotinib und Bevacizumab beim fortgeschrittenen NSCLC
Frankfurt am Main (9. November 2010) – Die frühzeitige und konsequente Behandlung mit Erlotinib (Tarceva®) und Bevacizumab (Avastin®) verbessert die Prognose beim fortgeschrittenen nicht-kleinzelligen Lungenkarzinom (NSCLC). Dies belegen eindrucksvoll die beim 35. Jahreskongress der European Society for Medical Oncology (ESMO) präsentierten Daten der Phase-III-Studie OPTIMAL sowie neue Analysen der SAiL-Studie.
Bei fortgeschrittenem Lungenkrebs: Die Tablette nach der Chemotherapie
Hamburg (5. Mai 2010) – Ab sofort können Lungenkrebs-Patienten, bei denen die erste Chemotherapie keinen Rückgang des Tumors, sondern lediglich einen Wachstumsstillstand bewirkt hat, früher von der Tablette Erlotinib profitieren. Sie erhalten den Wachstumshemmer direkt im Anschluss an die Chemotherapie. Diese neue Behandlungsstrategie kann helfen, das Fortschreiten der Erkrankung aufzuhalten und die Überlebenszeit der
WEITERLESEN »
Jetzt zugelassen: Tarceva in der 1st-Line-Erhaltungstherapie des fortgeschrittenen NSCLC
Hamburg (5. Mai 2010) – Am 27. April hat der orale EGFRInhibitor Erlotinib (Tarceva®) die europaweite Zulassung für die 1st-Line-Erhaltungstherapie bei Patienten mit lokal fortgeschrittenem oder metastasiertem NSCLC (Stadium IIIB/IV) mit Krankheitsstabilisierung („stable disease“) nach platinbasierter 1st-Line-Chemotherapie erhalten. Lungenkrebspatienten können nun früher von Erlotinib profitieren. Die Zulassung basiert auf den positiven Ergebnissen der Phase-III-Studie
WEITERLESEN »
Fortgeschrittenes NSCLC – Neue S3-Leitlinie empfiehlt Bevacizumab
Grenzach-Wyhlen (7. April 2010) – Die kürzlich veröffentlichte S3-Leitlinie „Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms“ empfiehlt Bevacizumab (Avastin®) zur First-Line-Therapie des fortgeschrittenen NSCLC. Denn zusammen mit einer platinbasierten Kombinationschemotherapie führt Bevacizumab zu einer signifikanten Verbesserung der Remissionsrate und der medianen Überlebenszeit bzw. des medianen progressionsfreien Überlebens, so die Begründung in der Leitlinie. Damit
WEITERLESEN »
Zielgerichtete Therapie des fortgeschrittenen NSCLC
Berlin (26. Februar 2010) – Beim fortgeschrittenen NSCLC zählt die zielgerichtete Therapie mit Erlotinib (Tarceva®) oder Bevacizumab (Avastin®) heute zu den etablierten Therapieoptionen und wird daher in der kürzlich publizierten interdisziplinären S3-Leitlinie empfohlen. Eine weitere Verbesserung der Therapieergebnisse lassen die beim Deutschen Krebskongress präsentierten Daten der SATURN (Sequential Tarceva in Unresectable NSCLC)-Studie erwarten. Danach profitieren
WEITERLESEN »
Kombination aus Pemetrexed/Cisplatin als ein Standard in der Erstlinientherapie des nicht-plattenepithelialen NSCLC anzusehen
Berlin (25. Februar 2010) – Die medikamentöse Behandlung von Patienten mit fortgeschrittenem nicht-kleinzelligem Lungenkarzinom (NSCLC) wird heute nach den individuellen histologischen Merkmalen des Tumors ausgewählt. Damit kann sichergestellt werden, dass die Patienten eine jeweils effektive Therapie erhalten. So kann sich bei Patienten mit dem histologischen Befund eines Nicht-Plattenepithel-karzinoms (Adeno- und großzelliges Karzinom) ein signifikanter
WEITERLESEN »
Epidemiologische Registerstudie an 6.000 NSCLC-Patienten gestartet
Hamburg (17. Dezember 2009) – Mit der Aufnahme der ersten Patienten in die REASON-Studie wurde in Deutschland jetzt eine der umfangreichsten epidemiologischen Registerstudien zum nicht-kleinzelligen Bronchialkarzinom (non-small cell lung cancer, NSCLC) gestartet. Am 13. November wurde das letzte von drei initialen Prüfertreffen erfolgreich durchgeführt. Damit ist ein Großteil der teilnehmenden Zentren bereit für den
WEITERLESEN »
Cisplatinbasierte Erstlinientherapie mit Pemetrexed verlängerte Überleben bei Patienten mit Adenokarzinom auf median 12,6 Monate
Bad Homburg (26. November 2009) – Erstmals verlängerte eine cisplatinhaltige Dublette studiengebunden die mediane Überlebenszeit von Patienten mit fortgeschrittenem Adenokarzinom auf über ein Jahr: Mit dem Behandlungsregime Pemetrexed (Alimta®) in Kombination mit Cisplatin in der Erstlinientherapie überlebte dieses Patientenkollektiv median 12,6 Monate gegenüber 10,9 Monaten unter Gemcitabin/Cisplatin. Die Daten gehen aus einer vorab geplanten
WEITERLESEN »
Personalisierte Therapie des fortgeschrittenen NSCLC
Berlin (23. September 2009) – Patienten mit nicht-kleinzelligem Lungenkarzinom (NSCLC) können heute auch im fortgeschrittenen Stadium langfristig überleben. Entscheidend dazu beigetragen haben die zielgerichteten Therapien mit Erlotinib (Tarceva®) und Bevacizumab (Avastin®), deren Wirksamkeit und Sicherheit in mehreren großen Phase-III- und -IV-Studien belegt ist. Welche Patienten im Versorgungsalltag von dem oralen EGFR-Inhibitor und dem Anti-VEGF-Antikörper
WEITERLESEN »
Überlegenheit von IRESSA in der Erstlinientherapie des NSCLC
Wedel (21.August 2009) – Das New England Journal of Medicine (NEJM) hat detaillierte Daten der Phase-III-Studie IPASS (IRESSA Pan-Asia Study) veröffentlicht. In dieser Studie wird IRESSA (Gefitinib) mit einer Doublet-Chemotherapie als Erstlinientherapie des fortgeschrittenen nicht-kleinzelligen Bronchialkarzinoms (NSCLC) verglichen. Die Ergebnisse belegen eine signifikant bessere Wirksamkeit zugunsten des EGFR-Tyrosinkinase-Inhibitors. Das Risiko für eine Krankheitsprogression durch
WEITERLESEN »
SATURN-Studie
Grenzach-Wyhlen (13. August 2009) – Aktuelle Daten der SATURN-Studie bestätigen eine signifikante Verlängerung des Gesamtüberlebens durch die Erhaltungstherapie mit Erlotinib (Tarceva®) bei Patienten mit metastasiertem oder fortgeschrittenem nicht-kleinzelligen Lungenkarzinom (non small cell lung cancer, NSCLC). Die neuen Studiendaten wurden auf der 13. World Conference on Lung Cancer (WCLC) vorgestellt. Dieser internationale Ärztekongress fand vom
WEITERLESEN »
Interview mit PD Dr. Jan Stöhlmacher: Fokus: Individualisierung der Krebstherapie
Bad Homburg (27. Juli 2009) – Die Individualisierung der Therapie beim nicht-kleinzelligen Lungenkarzinom (NSCLC) gewinnt im Praxisalltag zunehmend an Bedeutung. Mit der Einführung innovativer Substanzen haben Onkologen die Möglichkeit, ein möglichst maßgeschneidertes Behandlungskonzept mit effektiven Therapieaussichten für den einzelnen Patienten zu wählen. Für den Austausch zu aktuellen Onkologiethemen zwischen Ärzten und Wissenschaftlern fokussierte sich
WEITERLESEN »