MEDIZIN
AWARDS
Forschergeist gefragt: 14. Novartis Oppenheim-Förderpreis für MS-Forschung ausgelobt
FernstudiumCheck Award: Deutschlands beliebteste Fernhochschule bleibt die SRH Fernhochschule
Vergabe der Wissenschaftspreise der Deutschen Hochdruckliga und der Deutschen Hypertoniestiftung
Den Patientenwillen auf der Intensivstation im Blick: Dr. Anna-Henrikje Seidlein…
Wissenschaft mit Auszeichnung: Herausragende Nachwuchsforscher auf der Jahrestagung der Deutschen…
VERANSTALTUNGEN
Wichtigster Kongress für Lungen- und Beatmungsmedizin ist erfolgreich gestartet
Virtuelle DGHO-Frühjahrstagungsreihe am 22.03. / 29.03. / 26.04.2023: Herausforderungen in…
Pneumologie-Kongress vom 29. März bis 1. April im Congress Center…
Die Hot Topics der Hirnforschung auf dem DGKN-Kongress für Klinische…
Deutscher Schmerz- und Palliativtag 2023 startet am 14.3.
DOC-CHECK LOGIN
Nicht-kleinzelliges Lungenkarzinom (NSCLC)
Laut Zulassungsstudie verzögert Afatinib* nicht nur die Tumorprogression, sondern steigert auch Lebensqualität und bessert tumorassoziierte Symptome
Wien, Österreich (29. September 2012) – Eine aktuelle Auswertung der Lux-Lung 3 Studie unterstreicht, dass Patienten mit einem fortgeschrittenem nicht-kleinzelligen Lungenkarzinom (NSCLC) und Mutationen im Epidermal Growth Factor Receptor (EGFR) von einer Erstlinienbehandlung mit Afatinib* profitieren können. Die auf dem Kongress der European Society for Medical Oncology (ESMO) 2012 in Wien präsentierten Daten zeigen, dass Afatinib* im Vergleich zu einer Kombinationschemotherapie aus Cisplatin und Pemetrexed nicht nur die Tumorprogression signifikant verzögert. Vielmehr weisen die Patienten unter dem irreversiblen ErbB-Family-Blocker auch eine bessere Lebensqualität auf als diejenigen unter der gewählten Vergleichschemotherapie (p<0,05). Zudem ermöglicht Afatinib* eine signifikant effektivere Kontrolle der tumorassoziierten Symptome.
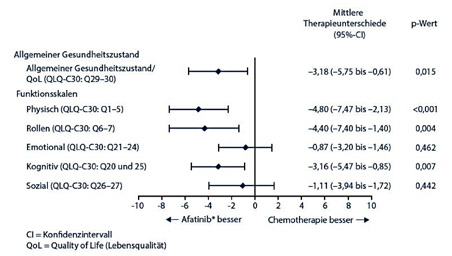
Die Erstlinientherapie mit Afatinib* steigerte in der LUX-Lung 3 Studie, einer multizentrischen, randomisierten, offenen Phase-III-Studie, die Lebensqualität signifikant gegenüber der für die untersuchte Patientenpopulation derzeit als beste angesehene Chemotherapiekombination aus Cisplatin und Pemetrexed [1}. Zur Erfassung der Lebensqualität und der tumorassoziierten Symptome wurden die Patienten um die Beantwortung zweier standardisierter Fragebögen gebeten: dem Fragebogen QLQ-C30 der European Organization for Research and Treatment of Cancer (EORTC) und dem lungenkrebsspezifischen Fragebogen EORTC QLQ-LC13. Die Teilnehmer füllten die Fragebögen zu Studienbeginn und im Weiteren alle drei Wochen bis zur Krankheitsprogression aus. Besonders erwähnenswert ist eine Compliance von über 85% hinsichtlich der Beantwortung und des Rücklaufs der Fragebögen [2]. Dabei zeigte sich, dass Afatinib* gegenüber der Chemotherapie signifikant besser abschneidet als die Vergleichstherapie; das betraf nicht nur die Lebensqualität insgesamt (p=0,015), sondern auch die physischen (p<0,001) und kognitiven Funktionen (p=0,007) sowie die Rollenfunktion (p=0,004) (Abb. 1) [2]. Hervorzuheben ist in diesem Zusammenhang die Bedeutung der verbesserten Lebensqualität für den Patienten durch den Erhalt der eigenständigen Lebensführung, die Teilnahme am Arbeits- und/oder Alltagsleben sowie die Ausübung von Freizeitaktivitäten.
![Abb. 1: Bessere Lebensqualität unter Afatinib* gegenüber Cisplatin/Pemetrexed in der LUX-Lung 3 Studie. Die Lebensqualität wurde mithilfe der Fragebögen EORTC QLQ-C30 und EORTC QLQ-LC13 erfasst (modifiziert nach [2]).](https://www.krankenpflege-journal.com/wp-kpj/wp-content/uploads/2012/09/Abb_1.jpg)
Abb. 1: Bessere Lebensqualität unter Afatinib* gegenüber Cisplatin/Pemetrexed in der LUX-Lung 3 Studie. Die Lebensqualität wurde mithilfe der Fragebögen EORTC QLQ-C30 und EORTC QLQ-LC13 erfasst (modifiziert nach [2]).
Bessere Kontrolle tumorassoziierter Symptome mit Afatinib*
Die Patienten unter Afatinib* (n=230) bewerteten nicht nur ihre Lebensqualität besser als die Patienten unter der Kombinationschemotherapie (n=115), auch eine klinisch relevante Besserung erkrankungsspezifischer Symptome kam unter Afatinib* häufiger vor: Husten 67% versus 60% (p=0,2444); Dyspnoe 64% versus 50% (p=0,0103) und Schmerz 59% versus 48% (p=0,0513) (Abb. 2) [2].
![Abb. 2: Eine Besserung der tumorassoziierten Symptome tritt mit Afatinib* häufiger auf als bei einer Cisplatin/Pemetrexed-Behandlung (modifiziert nach [2]).](https://www.krankenpflege-journal.com/wp-kpj/wp-content/uploads/2012/09/Abb_2.jpg)
Abb. 2: Eine Besserung der tumorassoziierten Symptome tritt mit Afatinib* häufiger auf als bei einer Cisplatin/Pemetrexed-Behandlung (modifiziert nach [2]).
Darüber hinaus verzögerte sich die Verschlechterung bzw. das Auftreten der tumorassoziierten Beschwerden Husten (Hazard Ratio [HR] 0,60; p=0,0072) und Dyspnoe (HR 0,68; p=0,0145) in der Afatinib*-Gruppe gegenüber der Chemotherapie-Gruppe signifikant (Abb. 3); für die tumorbedingten Schmerzen zeigte sich ein Trend zugunsten Afatinibs* (HR 0,82; p=0,1913). Insgesamt geht demnach die mit Afatinib* erzielte Verlängerung des progressionsfreien Überlebens auch mit besseren Lebensbedingungen für die Patienten einher, die sich zusätzlich in einer effektiven Symptomkontrolle äußern [2]. Dabei spiele gerade die Kontrolle der Beschwerden und die Lebensqualität für die Patienten eine enorm wichtige Rolle, wie Prof. Vera Hirsh, Onkologin an der McGill University und dem Royal Victoria Hospital in Montreal, Kanada, auf einer Pressekonferenz von Boehringer Ingelheim im Rahmen der ESMO-Tagung 2012 betonte.
![Abb. 3: LUX-Lung 3: Zeit bis zur Verschlechterung der Symptome Husten (a) und Dyspnoe (b) sowie Schmerz (c) (modifiziert nach [2]).](https://www.krankenpflege-journal.com/wp-kpj/wp-content/uploads/2012/09/Abb_3.jpg)
Abb. 3: LUX-Lung 3: Zeit bis zur Verschlechterung der Symptome Husten (a) und Dyspnoe (b) sowie Schmerz (c) (modifiziert nach [2]).
Patienten mit häufigen EGFR-Mutationen: Fast zweimal länger progressionsfrei mit Afatinib*
Für eine gute Wirksamkeit von Afatinib* sprach bereits die erste Auswertung der LUX-Lung 3 Studie, die auf der Jahrestagung der American Society of Oncology (ASCO) 2012 vorgestellt wurde: Darin betrug das mediane progressionsfreie Überleben (PFS) der Patienten mit einem Adenokarzinom der Lunge und positivem EGFR-Mutationsstatus unter Afatinib* 11,1 Monate, unter Pemetrexed und Cisplatin hingegen nur 6,9 Monate [3].
Besonders hervorzuheben sind die Ergebnisse für Patienten mit den häufigsten EGFR-Mutationen (del19 und L858R), die zusammen mehr als 90% aller Mutationen ausmachen [4]. Für diese Patientengruppe ließ sich unter Afatinib* nahezu eine Verdopplung des medianen progressionsfreien Überlebens (PFS) erzielen: In einer unabhängigen Auswertung lag das mediane progressionsfreie Überleben unter einer Afatinib*-Therapie bei 13,6 Monaten, unter Pemetrexed und Cisplatin blieben die Patienten im Median nur 6,9 Monate progressionsfrei (Abb. 4) [3].
Dabei geht die hohe Wirksamkeit von Afatinib* mit einem erwarteten Nebenwirkungsprofil einher, das zudem gut zu handhaben ist. Das bestätigte jetzt auch die auf dem ESMO 2012 vorgestellte Analyse von LUX-Lung 3 zur Lebensqualität [2, 3].
![Abb. 4: Medianes PFS der Patienten mit häufigen EGFR-Mutationen in der LUX-Lung 3 Studie (unabhängige Auswertung) (modifiziert nach [3]).](https://www.krankenpflege-journal.com/wp-kpj/wp-content/uploads/2012/09/Abb_4.jpg)
Abb. 4: Medianes PFS der Patienten mit häufigen EGFR-Mutationen in der LUX-Lung 3 Studie (unabhängige Auswertung) (modifiziert nach [3]).
LUX-Lung 3 ist eine große und robuste Studie beim EGFR-mutierten NSCLC
Die multizentrische, randomisierte, offene Phase-III-Studie LUX-Lung 3 ist mit 345 Teilnehmern eine große und robuste Studie zur Therapie des fortgeschrittenen NSCLC mit positivem EGFR-Mutationsstatus, wie Hirsh auf der Pressekonferenz weiter betonte. Sie ist zudem die erste Studie zur Erstlinientherapie, in der die für diese Patientengruppe derzeit als beste angesehene Chemotherapie aus Cisplatin und Pemetrexed als Vergleich dient (1). LUX-Lung 3 wurde weltweit durchgeführt und ihre Ergebnisse wurden zusätzlich von einer unabhängigen Kommission bewertet.
Klinisches Ansprechen auf Afatinib* auch bei „Uncommon Mutations“
Eine weitere Analyse der LUX-Lung 3 Studie, die ebenfalls auf dem ESMOJahrestreffen präsentiert wurde, belegt, dass Afatinib* auch bei Patienten mit „Uncommon Mutations“ wirksam ist. Derartige Mutationen – dazu gehören die Punktmutationen T790M, G719X, S768I und L861Q sowie Insertionen im Exon 20 des EGFR-Gens – wurden bei insgesamt 37 Patienten (10,7%, 26 Patienten im Afatinib*- Arm, 11 im Cisplatin/Pemetrexed-Arm) beobachtet. Abhängig von der vorliegenden Mutation konnte unter Afatinib* ein PFS von bis zu 19,2 Monaten (zensiert) erreicht werden. Weiterhin führte Afatinib* bei 19 von 23 Patienten mit messbaren Tumorläsionen zu einer Tumorverkleinerung [5].
Unter Berücksichtigung der kleinen Patientenzahlen führt Afatinib* demnach auch bei Patienten mit „Uncommon Mutations“ zu einem nach RECISTKriterien messbaren Ansprechen und einer verbesserten Krankheitskontrolle [5]. Dies bestätigt die Ergebnisse der vorangegangenen Phase-IIStudie LUX-Lung 2 [6].
Überprüfen des EGFR-Mutationsstatus sollte Standard vor Therapiebeginn werden
Die hier vorgestellten Ergebnisse der LUX-Lung 3 Studie demonstrieren, dass die frühzeitige Untersuchung des EGFR-Mutationsstatus (vor Therapiebeginn) wesentlich ist für eine optimale Therapieentscheidung und die Wahl der bestmöglichen Therapie für den Patienten mit fortgeschrittenem NSCLC in der Erstlinie. Bei etwa 10–15% der Kaukasier und 40% der Asiaten mit einem NSCLC weist der Tumor EGFR-Mutationen auf. In 90% der Fälle handelt es sich um eine der beiden Mutationen del19 oder L858R [3, 4]. In verschiedenen Studien konnte gezeigt werden, dass Patienten mit aktivierenden EGFR-Mutationen von der Behandlung mit einem EGFR-Blocker profitieren [3, 7, 8]. Auch Hirsh betonte auf der Pressekonferenz, dass ein Test auf das Vorliegen aktivierender EGFRMutationen beim NSCLC genauso Standard werden sollte wie die HER2-Testung beim Mammakarzinom. Nur so könne den Patienten die bestmögliche Erstlinientherapie geboten werden.
Anmerkung
-
* Afatinib ist eine noch nicht zugelassene Substanz, die sich noch in der klinischen Entwicklung befindet. Ihre Wirksamkeit und Sicherheit sind noch nicht vollständig nachgewiesen.
Referenzen
-
Scagliotti G, Parikh P, von Pawel J et al. J Clin Oncol 2008; 26: 3543-3551
-
Sequist LV, Schuler M, Yamamoto N et al. ESMO 2012, Abstract & Poster #1229PD
-
Yang JC, Schuler MH, Yamamoto N et al. J Clin Oncol 2012; 30 (suppl; abstr LBA7500), Abstract & Oral Presentation
-
Murray S, Dahabreh IJ, Linardou H et al. J Thorac Oncol 2008; 3: 832-839
-
Yang JC, Schuler MH, Yamamoto N et al. ESMO 2012, Abstract & Poster #1252P
-
Yang JC, Shih JY, Su WC et al. Lancet Oncol. 2012; 13(5): 539-48.
-
Rosell R, Carcereny E, Gervais R et al. Lancet Oncol. 2012; 13: 239-246
-
Zhou C, Wu YL, Chen G et al. The Lancet Oncology 2011; 12: 735-742
Quelle: Pressekonferenz von Boehringer Ingelheim im Rahmen der 37. Jahrestagung der European Society for Medical Oncology am 29.09.2012 (hB).